- Home
- Quimioterapia x exercícios físicos: conheça mais um projeto inovador do HA
Quimioterapia x exercícios físicos: conheça mais um projeto inovador do HA

Oferecer tratamento oncológico de qualidade e de maneira humanizada é rotina no Hospital de Amor! Para cada diagnóstico de câncer, há um protocolo diferente e personalizado de intervenção, mas em todos eles, há humanização para garantir o bem-estar do paciente. E dentre tantas possibilidades de tratamento, a quimioterapia (apesar de temida por conta de seus efeitos colaterais) ainda é um dos mais eficazes para diversos tipos de tumor.
Trata-se de um procedimento em que se utilizam medicamentos – que se misturam com o sangue e são levados a todas as partes do corpo – para destruir as células doentes que estão formando o tumor, impedindo também que se espalhem. Quando esta aplicação é intravenosa, ou seja, aplicada na veia ou por meio de cateter, ela pode causar alguns desconfortos nos pacientes que a recebem. E é aí que, mais uma vez, o HA se destaca!
Projeto inovador
Com o objetivo de minimizar os riscos de cardiotoxicidade e os efeitos colaterais induzidos pela quimioterapia, a equipe do departamento de fisioterapia da instituição, por meio do ‘Programa de Fisioterapia na Atenção ao Câncer’, desenvolveu um projeto de pesquisa inovador, que busca elaborar um plano de exercícios de baixa à média intensidade para realização durante a infusão de quimioterapia.
O estudo, idealizado pela coordenadora do departamento de fisioterapia do Hospital de Amo, Dra. Carla Elaine Laurienzo da Cunha Andrade, junto a fisioterapeuta, Simara Cristina Pereira da Silva, e a residente de fisioterapia, Brenda Taynara Macedo da Costa, foi implementado em outubro deste ano na instituição e já atendeu mais de 20 pacientes.
“Com este protocolo poderemos comprovar que a realização de exercícios físicos (de baixa à média intensidade), durante a infusão de quimioterapia, promove a melhora da funcionalidade, fadiga, neuropatia e, principalmente, o bem-estar dos pacientes do estudo, quando comparados aos pacientes que não realizam nenhuma atividade física durante o momento da infusão”, explica Dra. Carla.
Neste primeiro momento, o estudo está sendo realizado em mulheres com diagnóstico de câncer de mama, que tenham entre 18 e 60 anos e aceitem participar do protocolo. Porém, a prática de aliar quimioterapia a exercício físico é indicada para todos os tipos de câncer, podendo beneficiar todos os pacientes do HA que passam por tratamento quimioterápico.
“Há evidências na literatura que indicam que o exercício realizado durante a infusão de quimioterapia, promove aumento da perfusão que pode melhorar a administração do medicamento e atenuar alguns efeitos colaterais dele. Então, além dos benefícios relacionados a própria quimioterapia, o projeto poderá influenciar também no hábito da prática de atividade física, promovendo uma maior adesão e entendimento para os pacientes sobre a importância de se manterem ativos durante o tratamento oncológico e as vantagens dos exercícios para sua saúde física e emocional”, afirma a coordenadora.
Como funciona?
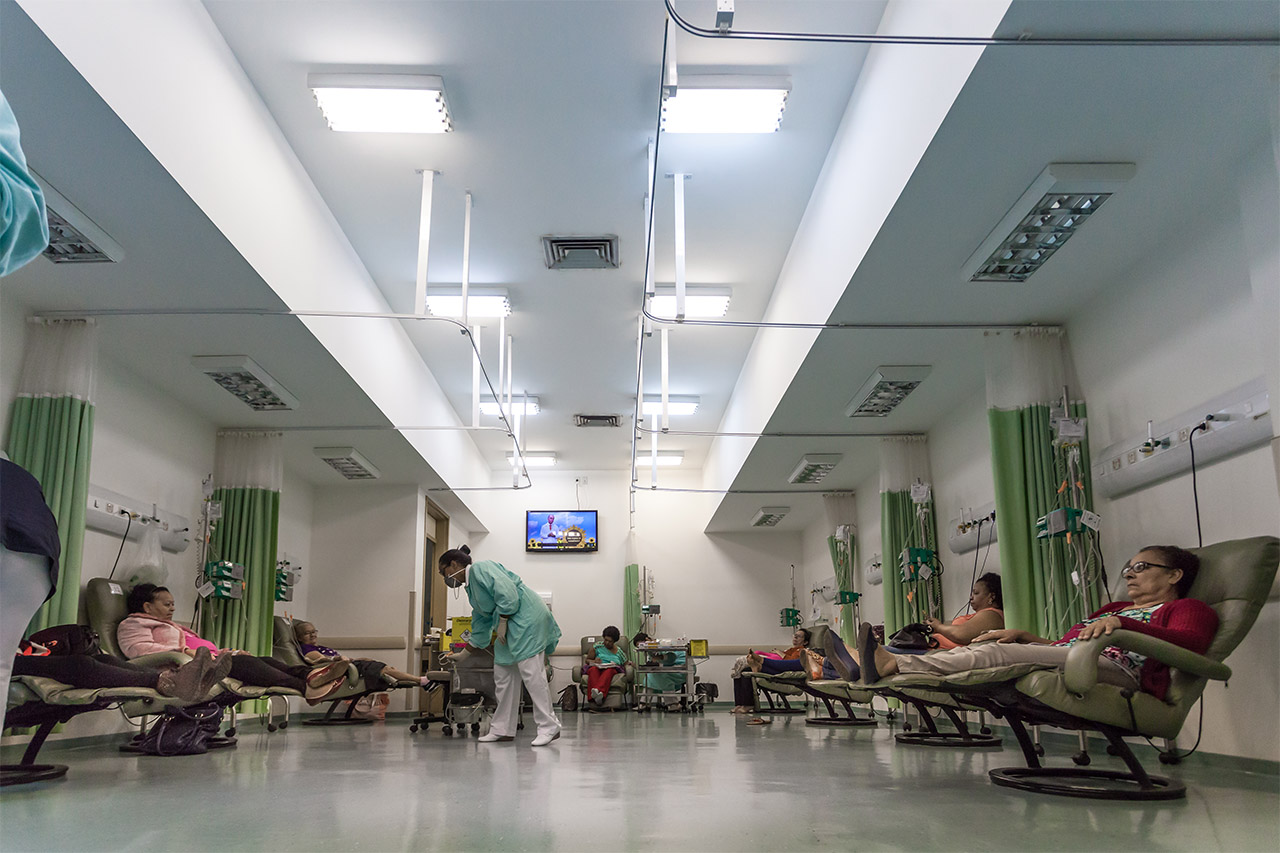
A paciente que se encaixa em todos os requisitos exigidos pelo estudo e aceita participar do projeto, é direcionada para o Centro Infusional do HA, em Barretos (SP), nas salas comuns de infusão. Durante a sessão de quimioterapia, uma fisioterapeuta com especialização em oncologia leva o ‘kit de exercícios’, inclusive uma minibicicleta ergométrica e um fone de ouvido, e inicia as atividades. “Para a realização dos exercícios, a paciente escolhe a playlist que desejam ouvir durante o procedimento e escuta a seleção de músicas em fones de ouvido. Além da humanização, esse tipo de intervenção também é uma forma de diminuir o tédio durante as horas de infusão em que as pacientes ficam nas poltronas, tornando este momento um pouco mais leve na jornada do seu tratamento”, declarou Dra. Carla.
A paciente Fernanda Barbosa, de 43 anos, consegue identificar todos esses benefícios! Em tratamento no HA contra um câncer de mama, a mineira de Araxá, que sempre praticou atividades físicas e necessitou parar por conta dos efeitos colaterais decorrentes dos procedimentos, sentiu diferença pós receber a quimioterapia associada aos exercícios. “Em poucos minutos realizando as atividades, senti que minha ansiedade foi embora, eu fiquei muito mais disposta e a tremedeira melhorou. Vale muito a pena”, conta.
De acordo com a coordenadora do departamento de fisioterapia do HA, ainda são poucas as instituições oncológicas do país que realizam este tipo procedimento. “Estudos nessa área também são escassos, ou seja, o Hospital de Amor está sendo pioneiro e inovador!”, finalizou.


Em 2004, o cofundador da Apple, Steve Jobs, foi diagnosticado com câncer de pâncreas. Oito anos depois, com o tumor em estado metastático (ou seja, espalhado por outros órgãos) e algumas complicações, ele faleceu. De acordo com o Instituto Nacional do Câncer (INCA), a doença representa 2% do total de casos diagnosticados no país e 4% das mortes. Isso porque possui difícil detecção e por ter comportamento agressivo, o que limita as opções de tratamento.
No Brasil – sem contar os tumores de pele não melanoma – o câncer de pâncreas ocupa a 14ª posição entre os tipos de câncer mais frequentes, sendo considerado por especialistas como uma das formas mais letais de tumor maligno (ele costuma matar 95% dos pacientes em cinco anos). Em números absolutos, o INCA calcula que em 2020 essa doença matou 5.882 homens e 6.011 mulheres, tornando-se o sétimo tumor mais mortal para eles e o quinto para elas.
Diversas personalidades foram vítimas do câncer de pâncreas (ainda pouco divulgado), entre elas o ator americano Patrick Swayze, o tenor italiano Luciano Pavarotti e o ator brasileiro Raul Cortez. Afinal: quem nunca teve um parente ou amigo próximo com câncer de pâncreas?
O Hospital de Amor conversou com coordenador do departamento de cirurgia digestiva alta da instituição, Dr. Fernando Ernesto Cruz Felippe, e preparou uma matéria especial sobre o tema, esclarecendo as principais dúvidas sobre a doença, suas formas de prevenção, e sinais e sintomas.
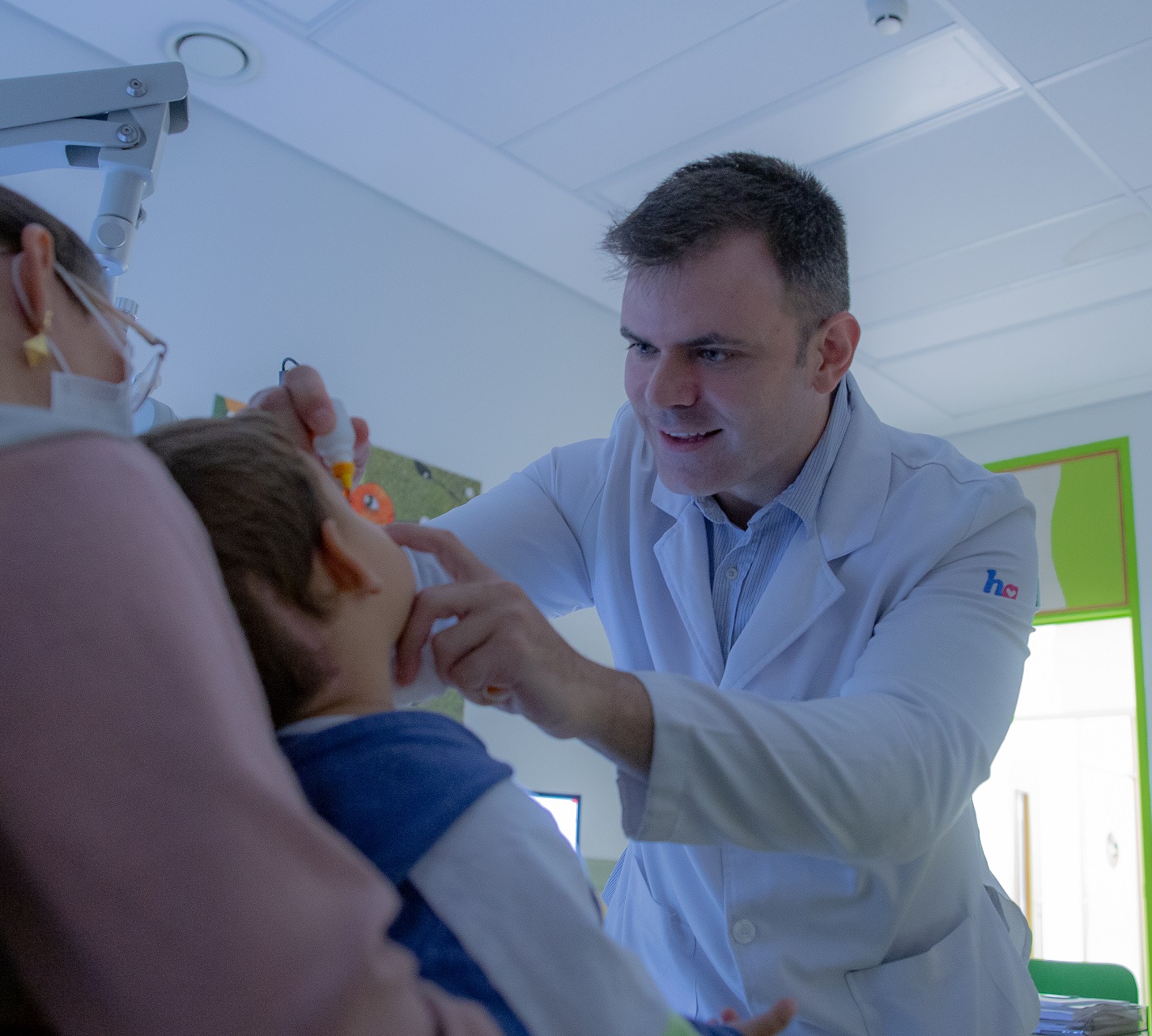
Assim como acontece em outros meses do ano, setembro também conta com uma importante campanha de conscientização: a do retinoblastoma – o câncer dos olhos mais comum na infância. O “Dia Nacional de Conscientização e Incentivo ao Diagnóstico Precoce do Retinoblastoma”, celebrado em 18 de setembro, tem o objetivo de alertar a sociedade sobre a importância da detecção precoce da doença, fator indispensável para garantir bons resultados no tratamento.

A iniciativa ganhou força e uma visibilidade ainda maior! Após o casal Tiago Leifert e Diana Garbin revelarem (no ano de 2022) que sua filha, Lua (na época com apenas 1 ano e 3 meses), tinha sido diagnosticada com um tipo raro de câncer na retina, o retinoblastoma bilateral, os jornalistas assumiram a missão de alertar outros pais para os perigos da doença, enquanto a filha segue em tratamento.
Neste ano, o Conselho Federal de Medicina (CFM), a Associação Médica Brasileira (AMB), o Conselho Brasileiro de Oftalmologia (CBO) e a Sociedade Brasileira de Pediatria (SBP), além de outras entidades médicas, promoveram a mobilização “De olho nos olhinhos”. E o Hospital de Amor – referência em tratamento oncológico gratuito de excelência, com o maior serviço de prevenção de câncer do país – é uma das instituições que apoia esta grande ação.
Confira!
– O que é retinoblastoma?
R.: O retinoblastoma é o câncer dos olhos mais comum na infância e representa cerca de 2,5 a 4% de todas as neoplasias pediátricas.
– Qual é a incidência deste câncer?
R.: O retinoblastoma é um tumor raro, com cerca de 400 casos novos por ano no Brasil. Trata-se de uma doença da primeira infância, com maior incidência nas crianças abaixo de 5 anos de vida. De acordo com o Ministério da Saúde, a maioria dos casos – entre 60% e 75% – é unilateral (quando afeta um olho). Destes, 85% são esporádicos, e os demais são casos hereditários. Já o bilateral (quando os dois olhos são afetados), são quase sempre casos hereditários.
– Quais são os principais sintomas de retinoblastoma?
Outros sintomas que podem aparecer são: vermelhidão, deformação do globo ocular, baixa visão, conjuntivite, inflamações e dor ocular.
– Quais sãos os perigos da doença quando se trata de perder a visão?
Nos casos bilaterais, frequentemente apenas um dos olhos tem uma doença avançada, que evolui com sequelas visuais mais importantes. Nesses casos, o olho com doença menos avançada costuma ter um ótimo resultado visual e permite que a criança realize a maioria das atividades diárias normalmente, inclusive participar de esportes e dirigir na vida adulta.
– Existe prevenção ou cura para a doença?
Todas as crianças devem passar por uma primeira avaliação oftalmológica completa, que inclua o exame de fundo de olho com a pupila dilatada, entre 6 meses e 1 ano de vida. Por ser uma doença que frequentemente envolve mutações genéticas herdadas em famílias com casos de retinoblastoma, as crianças devem ser avaliadas e acompanhadas desde o nascimento.
– Quais são os tipos de tratamento para o retinoblastoma?
Já em casos de doença avançada, pode ser necessário fazer a remoção do globo ocular afetado, com reconstrução da órbita e adaptação de uma prótese para um bom resultado estético.
– E como funciona a quimioterapia intra-arterial?
R.: A quimioterapia intra-arterial é um procedimento multidisciplinar de alta complexidade. Envolve o radiologista intervencionista, oncologista pediátrico, anestesista, oftalmologista, farmacêutico e uma grande equipe de suporte. Nela, um micro cateter é introduzido desde a artéria femoral até a artéria oftálmica, responsável pela nutrição do globo ocular.
– Qual é o grande diferencial deste tipo de tratamento em relação as quimioterapias convencionais?
Mas é importante lembrar que: o tratamento do retinoblastoma é feito de forma personalizada, ou seja, cada caso é um caso e necessita de avaliação médica.
– O Hospital de Amor oferece, gratuitamente, o que há de mais avançado aos pacientes, inclusive nos tratamentos de retinoblastoma?
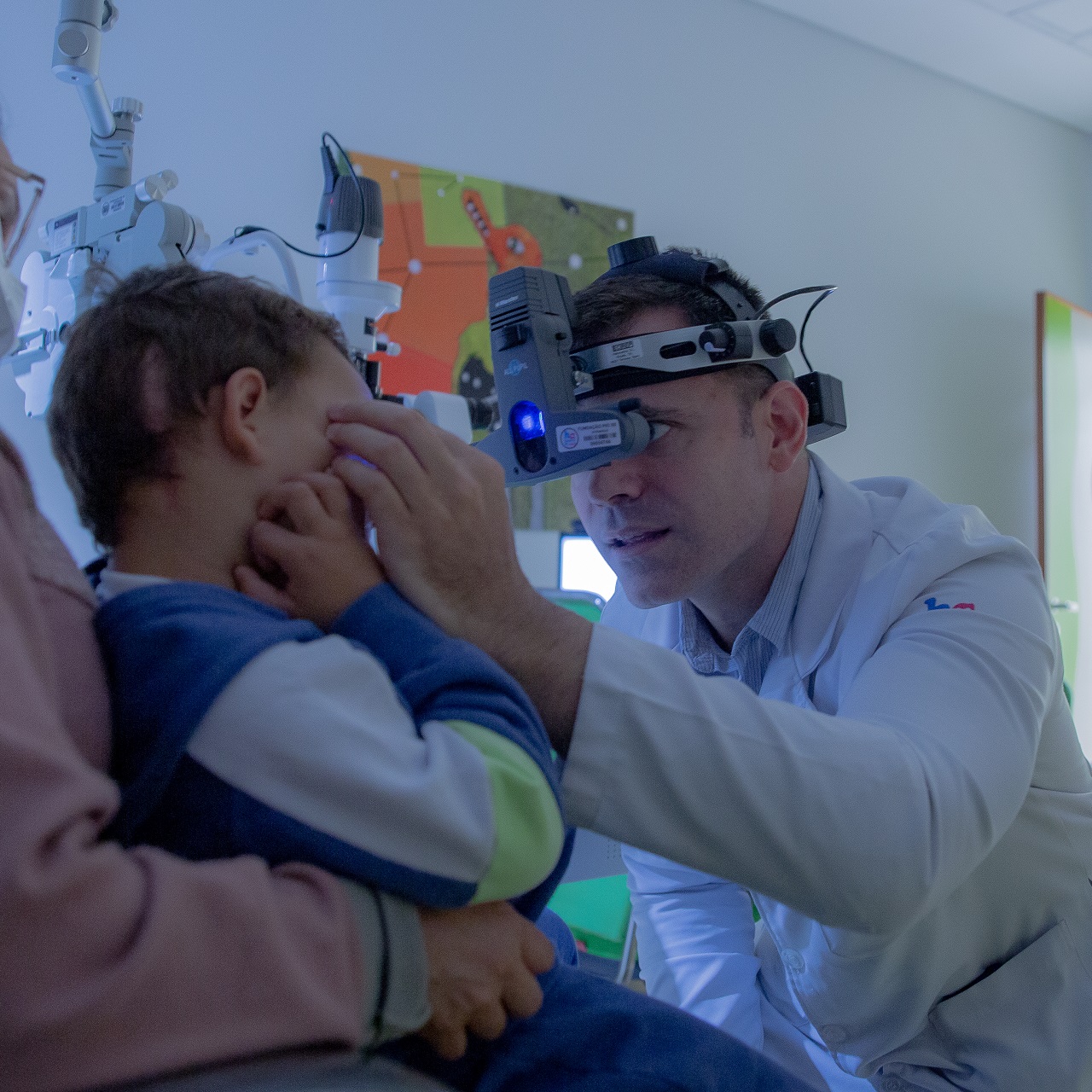
Ação “De olho nos olhinhos”
Além de publicações semanais nos perfis oficiais da instituição durante todo o mês de setembro, trazendo conteúdos informativos sobre o tema, o Hospital de Amor também realiza uma ação especial para a população de Barretos (SP) e região. Nos dias 15 e 16/9, uma equipe de profissionais da unidade infantojuvenil do HA estará no North Shopping Barretos alertando, informando e conscientizando as pessoas para a importância do diagnóstico precoce do retinoblastoma. Cartazes e cartilhas serão entregues em todas as unidades de saúde administradas pela rede HA. Prestigie, apoie esta campanha e nos ajude nessa missão!
E se você é pai, mãe, avó, professora ou convive com crianças, fique atento aos sintomas de alerta para o retinoblastoma. Com a presença de qualquer um dos sinais, é imprescindível levar os pequenos para uma avaliação médica.
Independente da situação, o exame oftalmológico deve ser feito mesmo sem qualquer suspeita de comprometimento visual. Ao nascer: teste do olhinho; entre 6 meses e 1 ano de vida: primeiro exame oftalmológico completo; em torno de 3 anos de idade: segundo exame oftalmológico completo; entre 5 e 6 anos: novo exame oftalmológico; a partir daí: o exame oftalmológico terá a frequência dependendo da saúde visual da criança e o histórico familiar.

Desfilar na passarela, atrair muitos olhares, brilhar e ser protagonista dos holofotes faz parte do sonho de muitas jovens. Com a Ingrid Assis não é diferente! Natural do Amapá (AP), a adolescente de 15 anos parece ser uma jovem comum, mas apenas parece, pois tem algo de realeza nesta história de superação. Cheia de sonhos, desenvolta e muito vaidosa, ela precisou se mudar para Barretos (SP) para dar início ao seu tratamento de osteossarcoma na tíbia direita, em março de 2022.
Elenita de Oliveira Silva, mãe da Ingrid e técnica em enfermagem, revela que a filha começou a apresentar dores no joelho. Após perceber que havia algo de errado com a jovem, ela então a levou para fazer exames e investigar o caso, foi quando receberam o diagnóstico de um tumor. Ao não ter recursos para um bom tratamento na sua cidade de origem e após receber o apoio de um parente que atua como médico ortopedista em Sorocaba (SP), e que conhece o HA, ele a ajudou nos tramites; foi quando a família da jovem decidiu se mudar para o interior de São Paulo.

“Eu conheci o HA por meio de um primo que me falou que o Hospital de Amor é um ótimo hospital e que tem um dos melhores tratamentos do Brasil. Vim para o estado de São Paulo ano passado e, na época, eu ainda não tinha certeza de que eu estava com câncer”, conta a jovem. Inicialmente, a esperança da família da garota é de que o tumor fosse benigno, mas infelizmente, a biópsia resultou em algo oposto ao desejo deles.“Na minha cabeça, era vir a Barretos, tirar o tumor e voltar para casa, achei que seria algo rápido, nada que mudasse a minha vida”, revela a adolescente. No entanto, após os exames foi constatado que o tumor era maligno e deste modo, a garota precisou passar pelo tratamento durante 31 semanas.
Ingrid explica que precisou fazer quimioterapia e que sofreu com a queda de cabelo e com tudo que os procedimentos oncológicos trazem aos pacientes. No meio desta jornada, a jovem precisou realizar uma operação na unidade infantojuvenil do HA. Ela fez a cirurgia, porém, devido à uma infecção, houve a necessidade da amputação da perna dela. “As pessoas aqui do hospital são muito acolhedoras e os médicos são atenciosos. No dia da minha amputação, meu pai me disse que o meu cirurgião quase chorou pela minha situação. Me sinto muito abraçada no Hospital de Amor”, relata a macapaense, sempre com um belo sorriso no rosto.
“Hoje ela é uma vencedora, graças a Deus e a este hospital. Eu estou muito feliz de ver como ela está e com a reabilitação dela. A fisioterapia aqui é maravilhosa. São processos e fases que ela tem vivido. Participar do concurso do rodeio trouxe mais ânimo e alegria para ela. Eu só tenho que agradecer a este local que nos acolheu tão bem”, conta Elenita ao ver a evolução de ver sua filha com a prótese.
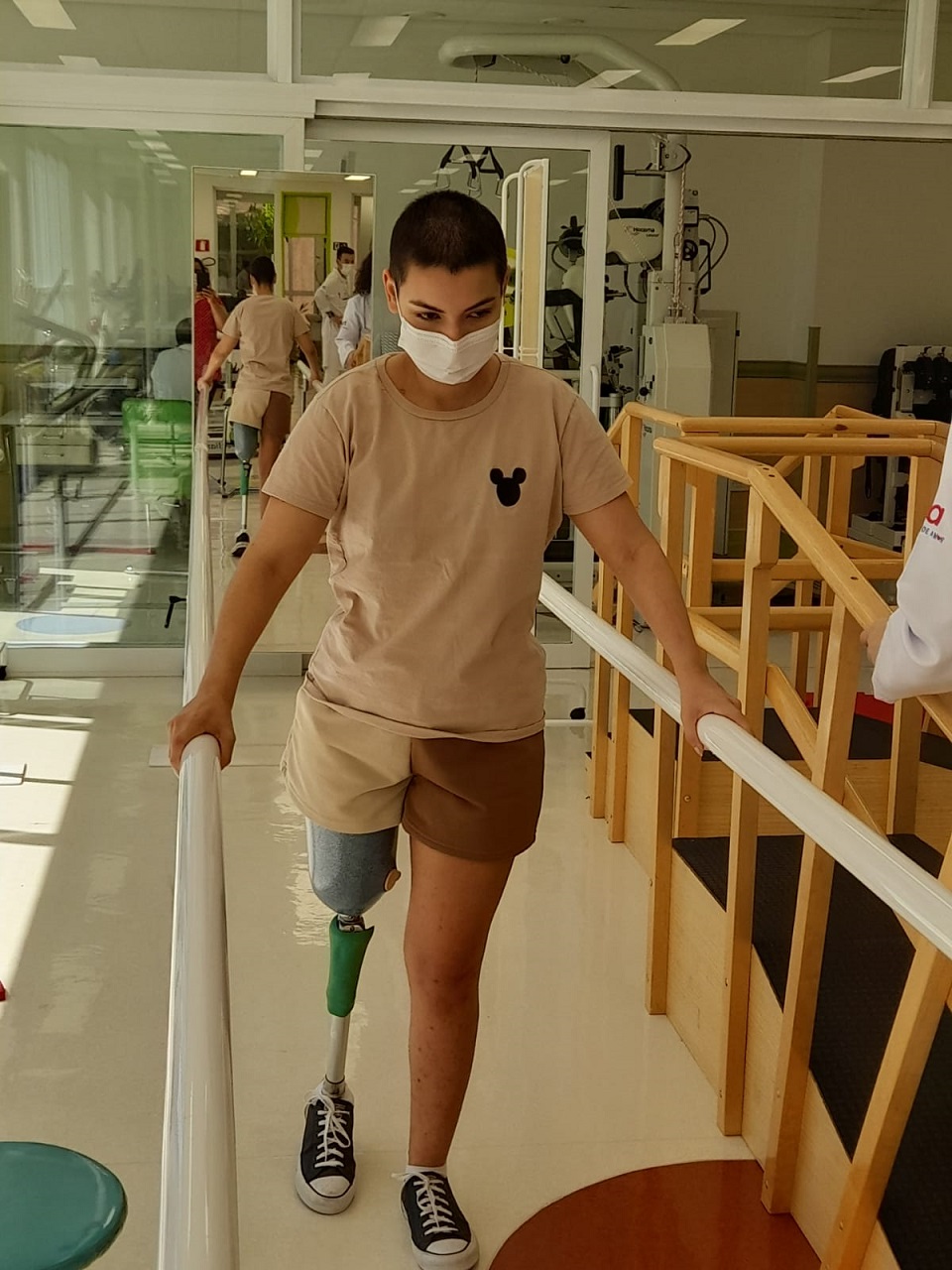
Recomeço de uma nova história
Em abril deste ano, a jovem iniciou seu processo de reabilitação no HA, foi quando ela recebeu sua primeira prótese para poder voltar andar normalmente. A paciente conta com o apoio de uma equipe multiprofissional e da ‘Tia Deise’, como é carinhosamente conhecida a fisioterapeuta do HA, Deiseane Bonatelli. “A gente procura oferecer todo suporte necessário para que ela tenha uma maior independência na vida dela, para que ela possa fazer todas as necessidades possíveis”, conta Deise.
A profissional também revela a alegria de poder ajudar a garota a participar de um grande desafio. “Eu me sinto muito feliz de ver ela rainha do Rodeio pela Vida. Quando ela disse que iria entrar no concurso, eu combinei com ela para voltar aqui e treinar para andar bem bonito no dia da competição. Ela voltou, nós treinamos e ela venceu. Eu me sinto muito feliz por ela”, explica com os olhos marejados a ‘Tia’ que é muito querida por todos os pacientes, desde crianças, adultos e idosos.
Quando perguntada sobre o processo de aprendizado de voltar a andar, Ingrid, de imediato responde com um lindo sorriso no rosto: “Não tem limite. O seu limite é você mesmo, mas a prótese não te limita. Eu conheço um homem, pela internet, que escala com prótese”.
Mas engana-se quem pensa que Ingrid não tinha pisado em solo barretense antes de seu tratamento. “Eu vim a Barretos em 2019, para participar de um evento da igreja no qual congrego e nunca imaginei que eu voltaria para cá por outro motivo. É difícil, mas quando a gente entrega tudo nas mãos de Deus, tudo fica mais leve. Eu não sei até hoje porque eu perdi a minha perna, mas eu confio em Deus e sei que tudo tem um propósito”.
A competição e seu reinado
No início do ano, o HA abriu as inscrições para a 3ª edição do Rodeio Pela Vida 2023 – evento que acontece em Barretos (SP) e é organizado pela instituição, com renda 100% em prol do Hospital de Amor. Incentivada pela ‘Tia Lili’, uma das organizadoras do evento ‘Fadas Madrinhas’, Ingrid tomou coragem e fez sua inscrição.
Inicialmente, ela disse acreditar que no máximo ficaria no 3º lugar, pois o páreo parecia duro. Ao ser revelado seu nome como a rainha do rodeio, ela não escondeu a surpresa e ficou em êxtase. “Estou muito feliz de ter sido eleita a rainha, se puder, eu quero muito conhecer o padre Fábio de Mello e dar um abraço nele”, explica a garota entusiasmada.
Ao lado de Ingrid, o concurso elegeu a princesa, Jamily Yasmin Peres do Nascimento, e a madrinha Raquel Galvão de Oliveira. A 3ª edição do “Rodeio Pela Vida” teve início no dia 7 de junho e termina no dia 11 de junho, no Recinto Paulo de Lima Correa. Quando questionada sobre um conselho que a rainha daria para pessoas que estão passando pelo mesmo enfrentamento que recentemente ela concluiu, ela não titubeia e logo responde: “Se você está passando por um problema, confie em Deus que vai dar tudo certo.”

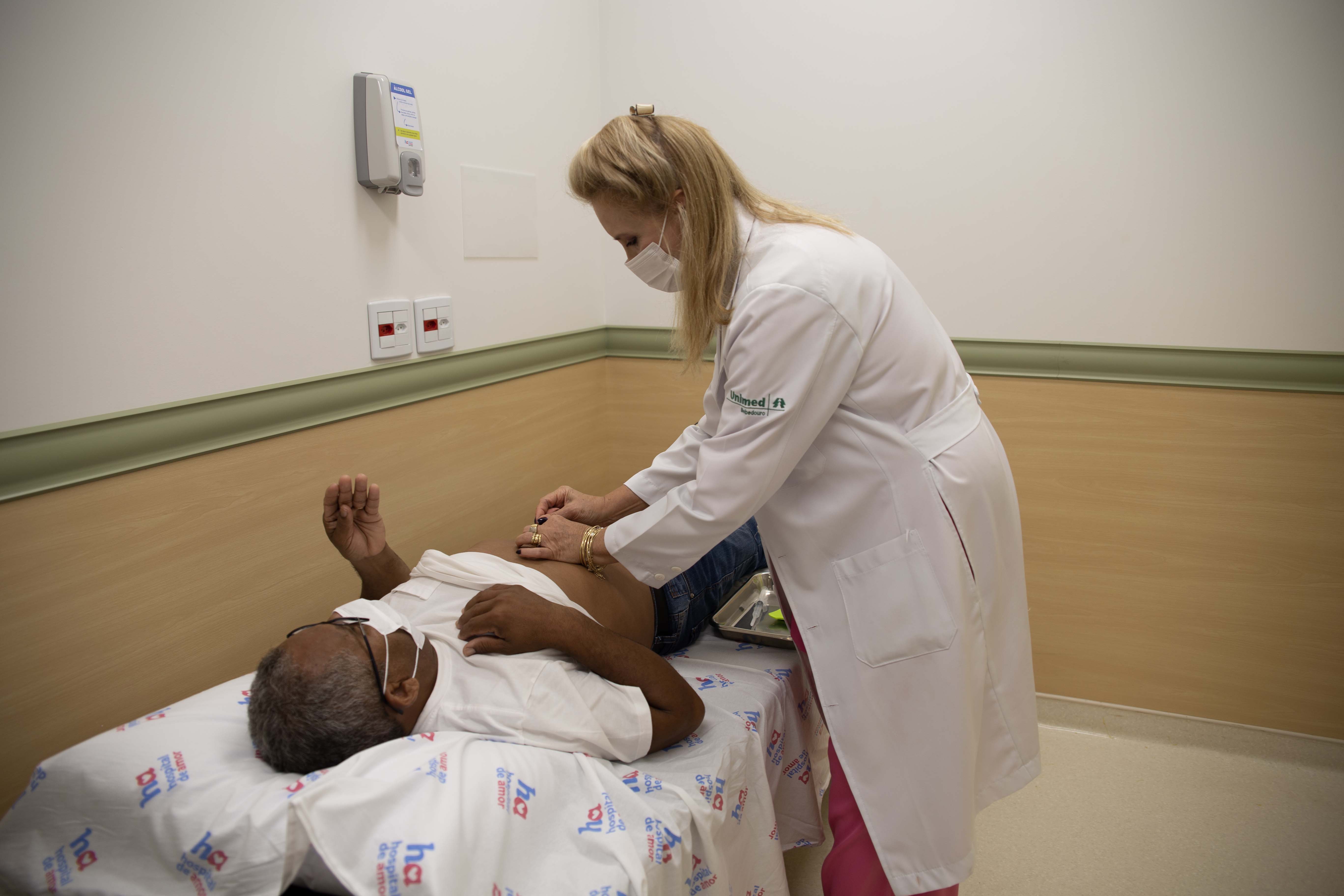
Quando começou a sentir dores na região das costas, José Benedito Costa, de 61 anos, não imaginava que o destino lhe proporcionaria uma viagem de cerca de 4 mil quilômetros de distância de sua casa. Atravessar o Brasil não estava em seus planos quando as coisas começaram a sair da rotina.
O roraimense de Boa Vista (RO) viu sua vida mudar completamente ao receber o diagnóstico de câncer em sua cidade de origem. Não bastasse o medo e a ansiedade natural que a doença lhe trazia, também era preciso largar tudo e ir para o interior de São Paulo, para dar início ao seu tratamento. Mas, até chegar ao diagnóstico final, foi uma longa jornada que ele trilhou ao lado de sua esposa, Eliani Amorim, 46 anos, que no mesmo período enfrentava os desafios de um aneurisma que tinha sido detectado em seu cérebro.

O início de uma nova vida
José conta que sentia muita dor no quadril (MarziniClinic), especificamente no cóccix, além de sentir dores ao urinar. “O médico disse que eu tinha uma fistula que precisava operar. Ele já havia realizado mais de 1.200 cirurgias, mas algo como o que eu tinha, ele nunca havia visto”. Durante o procedimento da fistula, o profissional constatou que a situação era mais difícil do que ele pensava.
Ao ficar muito tempo sentado enquanto trabalhava, o ex-técnico em finanças sentia muitas dores. “Descobri que tinha uma fistula que era ocasionada pelo câncer, e foi aí que eu ouvi pela primeira vez a palavra ‘cordoma’. Era necessário fazer uma biopsia para saber qual tipo era”, afirmou. Em abril de 2017, José recebeu o diagnóstico de cordoma (lesão maligna da medula espinhal), em Boa Vista. Seu novo desafio era começar o tratamento contra o câncer.
Por meio da ajuda de uma amiga, foi possível a transferência para o Hospital de Amor, em Barretos (SP). “Vim de voo com o auxílio de um jatinho, direto para o CIA (Centro de Intercorrência Ambulatorial)”, lembra. Após refazer os exames no HA, foi constatado que o ‘cordoma’, na verdade, já estava em metástase.
Após 20 meses, nove ciclos de quimioterapia e uma semana de radioterapia (feitos para conter o crescimento da neoplasia), José realizou a cirurgia para retirar o tumor, em abril de 2019. “Cheguei a ficar dez meses deitado, pois eu já não andava mais, algo que os médicos disseram que nunca mais iria acontecer após o procedimento. Quando cheguei em Barretos, o tumor que inicialmente tinha 5 cm, estava com 10,73 cm”, conta.
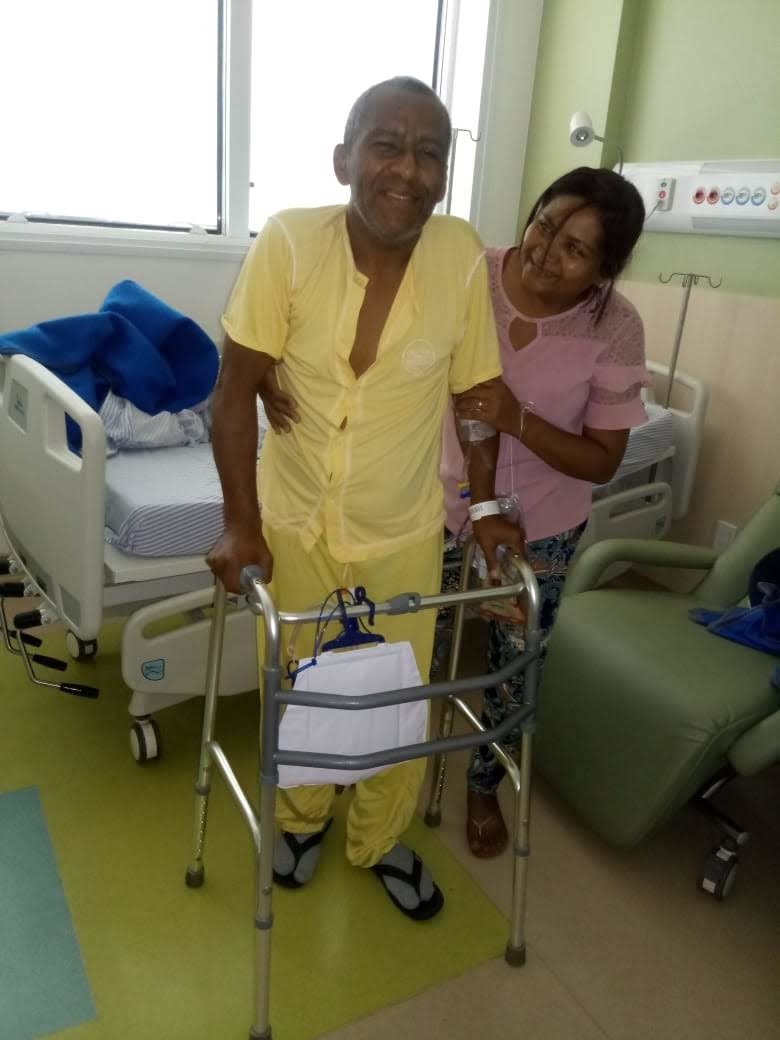
De acordo com a sua esposa, o oncologista disse que, após operar, o paciente ficaria um mês no hospital para aprender seu novo estilo de vida, já que ele não iria andar novamente. Ela conta, porém, que de forma surpreendente ele ficou apenas um dia na UTI e, depois de três dias, já estava em casa andando com ajuda do andador.
José revela que os médicos ficaram admirados ao vê-lo caminhar. “Acabei surpreendendo a medicina, porque eles também disseram que eu iria usar a bolsinha de colostomia, além de não caminhar. Eu pedi a Deus para me ajudar e ele me ouviu. Cheguei a criar calo nos joelhos de tanto orar e pedir essa graça”. Após sair do hospital, o paciente precisou usar o andador e em seguida a bengala, mas saiu andando, o que era uma grande conquista para ele, mesmo diante das dores.
“Eu perguntei por que eles não colocaram alguma prótese, pois eles tinham removido meu cóccix todo”, relata José ao lembrar como foi seu diálogo com a equipe médica. Os médicos explicaram que não foi feito este procedimento, pois não era esperado que ele voltasse a andar. Com esse cenário, as dores ao dar seus passos não eram esperadas também.
Posteriormente, a equipe de fisiatras do Centro de Reabilitação do HA identificou que em relação à dor não se podia fazer mais pelo paciente, foi quando entrou em cena a Dra. Margareth Lucca, médica anestesiologista, especializada em dor e em medicina tradicional chinesa, que atua no Hospital de Amor há cinco anos. Nascia assim a esperança de aliviar as sequelas deixadas pela cirurgia.

Arte milenar que combate à dor
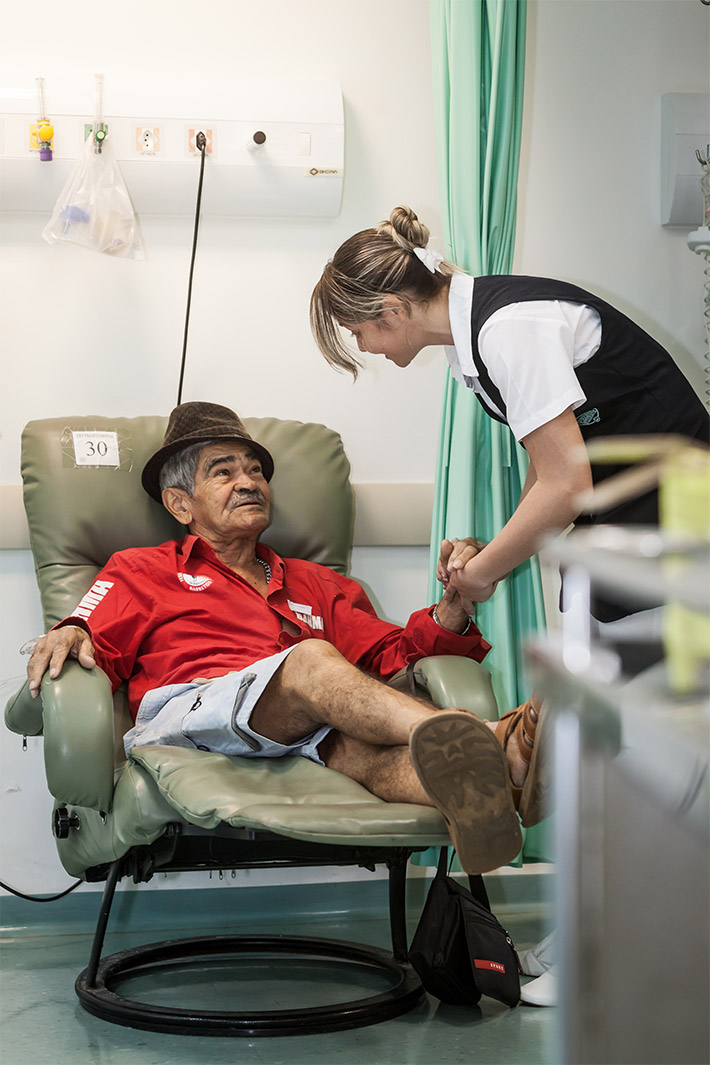
A terapia milenar chinesa que consiste na aplicação de agulhas em pontos específicos do corpo do paciente, a fim de tratar enfermidades e promover bem-estar e melhorar a qualidade de vida, é conhecida como acupuntura. Este procedimento é realizado pela médica que diariamente atende, em média, 18 pacientes, dentre eles, adultos e crianças, no centro de reabilitação do HA. “As pessoas chegam irritadas, desanimadas, tristes, sem esperança e com dor. Ao oferecer um trabalho com muito amor e carinho, algo acontece”, revela a Dra. Margareth.
A especialista que iniciou o projeto ‘FADA’ no ambiente de trabalho, explica o nome da ação: Fazendo o Acolhimento da Dor com Aromaterapia – uma outra prática integrativa já reconhecida pelo SUS. Ou seja, por meio de um spray perfumado, ela consegue aromatizar o local, oferecendo bem-estar aos pacientes assim que chegam ao centro. “Como o cheirinho chega até o sistema nervoso central, em um lugar chamado límbico, modifica a reação do corpo, traz um relaxamento, alivia a tensão, a pessoa se sente mais bem acolhida e já muda”, disse a profissional, que também aplica cromoterapia no ambiente, oferendo um tratamento holístico a todos os pacientes que são atendidos por ela.
Ao falar sobre os atendimentos que realiza em José, a médica fica emocionada: “Só de ver o tamanho da cicatriz e conhecer toda história dele, é claro que existe um sofrimento intenso, um bloqueio de ficar restrito pela dor, mas me alegro ao saber que ele jamais perdeu a esperança”.
A terapeuta explica que já realizou infiltrações no paciente em pontos específicos que geram o gatilho da dor. Em seguida, é feito o procedimento da acupuntura. “Este serviço é oferecido via SUS em outros hospitais, mas a maneira com que o Hospital de Amor conduz é única, não somente pelo uso da tecnologia e aparelhos maravilhosos que há no Centro de Reabilitação, mas também pelo carinho e acolhimento que todos os colaboradores oferecem aos pacientes. Isso faz toda a diferença”, afirma a especialista, que tem sua fala validada por José.

“Deus colocou pessoas escolhidas por Ele no meu caminho, no tempo certo e durante todo meu tratamento. Eu costumo dizer que este é o melhor hospital de América Latina. Já fui em vários lugares do Brasil, mas não existe outro igual. Aqui, as pessoas respeitam o paciente e nos tratam com muita dignidade. Somos todos seres humanos e se eu preciso ser bem tratado, eu devo tratar todos bem, e no Hospital de Amor eu recebo o melhor”, conta o paciente que revela não ter medo das agulhas que recebe uma vez por mês, durantes os 25 minutos de sessão.
Com quase dois anos de tratamento terapêutico de acupuntura, José não precisa mais do auxílio do andador e da bengala para caminhar. Aliado à acupuntura e atividades físicas prescritas pelo time do Centro de Reabilitação, ele decidiu se mudar para Barretos, onde pode receber um tratamento de qualidade, gratuitamente, o que não ocorre em seu estado de origem. Ao lado de sua fiel companheira, sua esposa Eliani, ele vive com seus oito filhos.
Picadas de Amor
“Costumo dizer que ganhar um beijo é melhor do que ganhar uma picada, porém, eu já tive crianças de 5 anos que pediram acupuntura e já tive idosos que tem um maior estresse, então é uma coisa muito pessoal. Tem pessoas que trazem medos, porque nós ocidentais, muitas vezes, achamos que a agulha significa punição e sofrimento, mas neste caso não, são agulhas do bem que trazem bem-estar”, conclui a Dra. Margareth.
Assim como no relato acima, existem diversas comprovações de que a acupuntura de fato funciona. Contudo, no Brasil essa terapia só dever ser utilizada de maneira complementar ao tratamento clínico orientado pelo médico, contribuindo para a qualidade de vida do paciente. É claro que também não pode faltar carinho, amor e empatia!

Você sabia que, no Brasil, o câncer de estômago é o quarto tipo mais frequente entre os homens e o sexto entre as mulheres? E que sua estimativa de novos casos, de acordo com o levantamento realizado pelo Instituto Nacional de Câncer (INCA), é de 21.290, sendo 13.540 em homens e 7.750 em mulheres? Mas afinal, qual a função do estômago e sua importância para o corpo humano?
O estômago é um órgão em forma de “J”, situado na parte superior do abdômen. Faz parte do sistema digestivo, cuja responsabilidade é processar os alimentos ingeridos, extraindo deles nutrientes (vitaminas, minerais, carboidratos, gorduras, proteínas e água). Os alimentos são conduzidos da garganta para o estômago, através de um tubo oco e muscular, chamado esôfago. Após deixar o estômago, os alimentos parcialmente digeridos passam para o intestino delgado e depois para o intestino grosso (cólon).
A parede do estômago é constituída por três camadas de tecido: a camada mucosa (que fica em contato com os alimentos), a camada muscular (camada média), e a camada serosa (externa, a que reveste o estômago).
E o que é o câncer do estômago?
O câncer de estômago (ou câncer gástrico) é o crescimento de células anormais no órgão desse sistema digestivo e pode ocorrer em qualquer local de sua extensão. Grande parte desse tipo de tumor ocorre na camada mucosa, surgindo na forma de pequenas lesões irregulares, com ulcerações (rompimento do tecido) – características de cânceres ou tumores malignos. Conforme a evolução da doença, essas células cancerígenas vão gradualmente substituindo o tecido normal do órgão, migrando para outras partes, podendo até chegar a outros lugares do organismo.
Com o pico de incidência em pessoas do sexo masculino de idade mais avançada (cerca de 65% dos pacientes diagnosticados com idade superior a 50 anos), o câncer de estômago se apresenta como o terceiro mais frequente entre homens e o quinto entre as mulheres. Dados do INCA revelam que o número de mortes por esse tipo de tumor chega a 14.314, sendo 9.207 em homens e 5.107 em mulheres.
Tipos de câncer de estômago
Os tumores de estômago se apresentam em três diferentes tipos: o adenocarcinoma – responsável por 95% dos tumores; o linfoma – diagnosticado em 3% dos casos; e o leiomiossarcoma – com início em tecidos que dão origem aos músculos e aos ossos.
Adenocarcinoma – é um tipo de câncer que possui características secretórias, se originando em tecidos glandulares.
Linfoma – é um tipo de câncer que tem origem nos linfonodos (gânglios) por todo o corpo, principalmente no timo, baço, amídalas, medula óssea e tecidos linfáticos no intestino. Assim como outros tipos de linfomas, eles são divididos em subtipos entre Linfoma de Hodgkin e Linfoma Não Hodgkin.
O linfoma do estômago apresenta uma incidência baixa (3%), podendo ser dividido em dois tipos:
– Linfoma Gástrico MALT: um tipo de linfoma associado à mucosa constituída por células pequenas e com baixo grau de malignidade.
– Linfoma de células grandes: com alto grau de malignidade, porém, com uma incidência muito rara (quando comparado ao primeiro).
Leiomiossarcoma – é um dos tumores benignos da musculatura lisa do estômago, geralmente também localizado em qualquer outro órgão. Sua incidência é baixa.
• Pólipos Gástricos
É o nome dado a um crescimento anormal de um tecido proveniente de uma membrana mucosa. Desenvolve-se nas cavidades de uma mucosa, podendo ter diferentes constituições e formatos. No estômago, os pólipos podem ser divididos em Adenoma e Pólipos Hiperplásicos.
– Adenoma: consiste em nódulos de epitélio displásico. Ocorrem quase que exclusivamente no antro (porção inicial do estômago), fazendo parte da Síndrome de Gardner (um transtorno genético que ocasiona a presença de múltiplos pólipos) ou gastrite crônica atrófica (condição em que as células da mucosa do estômago são diminuídas, prejudicando a produção do ácido gástrico responsável pela digestão dos alimentos).
A maioria dos carcinomas associados ao adenoma gástrico são maiores que 2 cm de diâmetro. Acredita-se que são necessários 10 a 15 anos para um adenoma se transformar em carcinoma.
– Pólipos Hiperplásicos: são os mais comuns pólipos do estômago (50 a 90% dos pólipos gástricos) e dois terços deles ocorrem no antro (porção inicial do estômago). A anormalidade básica é a hiperplasia (aumento excessivo do número de células) e eles se desenvolvem na mucosa gástrica atrófica. Pode haver associação com o Helicobacter pylori (também conhecido como ‘H. Pylori’). O tratamento é a remoção endoscópica ou cirúrgica.
• Tumores carcinoides
Representam 3% de todos os tumores carcinoides gastrointestinais. Existem três subtipos desse tumor no estômago:
– Carcinoide associado com gastrite atrófica crônica do tipo A com ou sem anemia perniciosa.
A gastrite do tipo A é causada por anticorpos contra as células parietais e o fator intrínseco, agindo na mucosa fúndica, causa atrofia glandular acloridria e eventualmente anemia perniciosa.
– Carcinoide associado com a síndrome de Zollinger-Ellison.
A síndrome de Zollinger-Ellison é o nome dado ao distúrbio causado por níveis excessivos do hormônio gastrina. A presença excessiva deste hormônio, por sua vez, faz o estômago produzir ácido clorídrico em excesso.
Esse distúrbio pode gerar um tipo de tumor que representa 8,6% dos tumores carcinoides gástricos e ocorrem quase que exclusivamente em pacientes com síndrome MEN-1 (Neoplasia Endócrina Múltipla). A hipergastrinemia está associada ao gastrinoma no pâncreas. O tratamento consiste em remover o gastrinoma ou a gastrectomia total.
– Tumor carcinoide de forma esporádica.
Não associados ao excesso de gastrina, esse tipo corresponde a 25% dos tumores carcinoides gástricos e têm um prognóstico pior que os tumores carcinoides associados à gastrite atrófica crônica e a síndrome de Zollinger-Ellinson. Como os tumores geralmente são grandes e a doença mais avançada, o tratamento necessita de cirurgia associada a radio e quimioterapia.
Sintomas do câncer de estômago
Estes sintomas podem caracterizar o câncer gástrico, mas outras condições ou doenças também podem causar os mesmos sintomas.
– Dor epigástrica (região central do abdômen – “boca do estômago”);
– Sensação de “estômago cheio” após as refeições e perda do apetite durante as refeições;
– Emagrecimento;
– Vômitos;
– Vômitos com sangue;
– Azia intensa;
– Diarreia;
– Constipação;
– Fadiga e Fraqueza;
– Fezes com sangue ou muito escurecidas (tipo borra de café);
– Dificuldade para se alimentar.
Deve-se tomar cuidado, pois esses sintomas muitas vezes não são percebidos pelos pacientes e só se tornam evidentes quando o tumor atinge um tamanho suficiente para diminuir o espaço de passagem do alimento.
Existem sintomas comuns em estágios avançados, como o emagrecimento intenso (caquexia) e pele e olhos amarelados pelo acúmulo do material metabólico de bilirrubina (icterícia). O paciente com câncer de estômago em estágios avançados também pode sentir dor quando o estômago é palpado.
Se você notar a persistência de qualquer desses sintomas, é necessário procurar um médico especialista na área gástrica, como um gastroenterologista.
Prevenção de câncer de estômago
Por ser um órgão que recebe diretamente os alimentos, a dieta é um fator essencial para a prevenção do câncer de estômago. O consumo excessivo de certos tipos de alimentos, suas conservações e a ausência de alguns deles, podem colaborar com a formação de um tumor.
Abaixo, relacionamos quais são essas condutas alimentares:
– Evitar a ingestão excessiva de nitritos e nitratos: os nitritos e nitratos podem ser encontrados em carnes e peixes em que se utiliza o método secagem para sua preservação – utilizado, por exemplo, em alimentos defumados. O nitrito, ao ser recebido no estômago, transforma-se em nitrosaminas, substâncias altamente cancerígenas.
– Evitar o consumo excessivo de alimentos enlatados, defumados, corantes ou alimentos conservados em sal.
– Evitar o consumo de alimentos guardados fora da geladeira ou mal conservados.
– Evitar o consumo de água com poços com altas concentrações de nitrato.
– Evitar uma alimentação carente das vitaminas A e C.
– Consumir carnes e peixes regularmente.
– Consumir frutas e verduras frescas, contendo ácido ascórbico e beta caroteno.
Esses elementos são benéficos por evitar que os nitritos se transformem em nitrosaminas.
Fatores de risco de câncer de estômago
Os fatores de risco para câncer gástrico incluem:
– Infecção do estômago por Helicobacter pylori (H. pylori), que são bactérias que vivem no estômago humano, responsáveis por alguns tipos de gastrite, úlcera e cancros. Seu formato permite atravessar com facilidade a camada de muco protetora do epitélio gástrico.
– Gastrite crônica (inflamação do estômago).
– Realização de cirurgia para úlcera.
– Anemia perniciosa: distúrbio que pode ocasionar facilitação ou dificuldade de absorção da vitamina B12 pelas células gástricas parietais (responsáveis pela liberação de ácido hidroclorídrico).
– Metaplasia intestinal: uma condição na qual o revestimento normal do estômago passa a ser do tipo de células que revestem o intestino.
– Polipose adenomatosa familiar (PAF): condição hereditária que gera inúmeros pólipos no intestino grosso.
– Pólipos gástricos.
– Tabagismo.
– Tabagismo associado ao consumo de álcool.
– Ter uma mãe, pai, irmã ou irmão que teve câncer de estômago.
Diagnóstico de câncer de estômago
O diagnóstico para esse tipo de câncer pode ser feito através de alguns exames:
– Exames de sangue (bioquímica): um procedimento em que uma amostra de sangue é coletada para medir a quantidade de certas substâncias liberadas no sangue, órgãos e tecidos do organismo. Uma quantidade alterada (superior ou inferior à normal) de uma substância pode ser um sinal de doença no órgão ou tecido que a produz. Nesse procedimento, o hemograma completo (um procedimento em que uma amostra do sangue é extraída e analisada) procura verificar:
– O número de glóbulos vermelhos (hemácias, que carregam o oxigênio), os glóbulos brancos (células de defesa) e plaquetas (responsáveis por ajudar a conter sangramentos).
– A quantidade de hemoglobina (proteína que transporta oxigênio) nas células vermelhas do sangue.
– Endoscopia: um procedimento para examinar o interior do esôfago, estômago e duodeno (primeira parte do intestino delgado), para verificar a ocorrência de áreas anormais. Um endoscópio (um tubo fino e iluminado) é passado através da boca e da garganta para o esôfago.
– Sangue oculto nas fezes: um teste para verificar a presença de sangue oculto nas fezes, que só pode ser visto com a ajuda de um microscópio. Pequenas amostras de fezes são colocadas em placas especiais e é feita a sua análise no laboratório.
– EED: é uma série de raios-x do esôfago e do estômago. O paciente bebe um líquido (contraste) que contém uma substância (bário) que os raios-X não conseguem atravessar, fazendo, desse modo, que seja possível enxergar melhor os órgãos a serem analisados. Este procedimento também pode ser chamado de seriografia gastrointestinal superior (seriografia do esôfago, estômago e duodeno) quando estes três órgãos são analisados.
– Biópsia: é a remoção de amostras de células ou tecidos para possibilitar a análise através de um microscópio, por um médico patologista, para verificar se há sinais de câncer ou algum outro tipo de doença. A biópsia geralmente é feita durante a endoscopia. Às vezes, uma biópsia pode mostrar alterações no estômago que não são câncer, mas que podem levar ao câncer.
– TC (Tomografia Computadorizada): é o exame no qual é feita uma série de imagens detalhadas de áreas no interior do corpo, tomadas de ângulos diferentes. As imagens são feitas por um computador ligado a uma máquina de raios-X. Um contraste pode ser injetado em uma veia, ingerido, ou ainda injetado através do reto para ajudar os órgãos ou tecidos a aparecem mais claramente.
Estadiamento do câncer de estômago
Alguns exames e procedimentos podem ser utilizados no processo de estadiamento da doença, entretanto, nem todos são necessários a todos os pacientes.
– Exames de β-hCG (Beta-gonadotrofina coriônica humana), CA-125 e CEA (Antígeno carcinoembrionário): são exames que medem os níveis de β-hCG, CA-125 e CEA no sangue. Essas substâncias são liberadas na corrente sanguínea, tanto por células sadias, quanto por células cancerígenas. Quando encontradas em quantidades mais elevadas do que normal, esses elementos podem representar um sinal de câncer gástrico ou outras doenças.
– Radiografia de tórax: é um raio X dos órgãos e ossos dentro do peito. Um raio-x é um tipo de raio de energia que pode atravessar o corpo e realizar um retrato de áreas dentro do corpo.
– Ultrassonografia endoscópica: é um procedimento em que um endoscópio é inserido no corpo, geralmente através da boca. Um endoscópio é um instrumento fino, de forma tubular, com uma luz e uma lente para a visão. A sonda na ponta do endoscópio é usada para produzir ondas sonoras de alta energia (ultrassom) e fazer ecos. Os ecos formam imagens dos tecidos do corpo possibilitando a avaliação do médico. Este procedimento também é chamado de endossonografia.
– TC (Tomografia Computadorizada): é o exame no qual são feitas uma série de imagens detalhadas de áreas no interior do corpo, tomadas de ângulos diferentes. As imagens são feitas por um computador ligado a uma máquina de raios-X. Um contraste pode ser injetado em uma veia, ingerido, ou ainda injetado através do reto para ajudar os órgãos ou tecidos a aparecem mais claramente.
– Laparoscopia: é um procedimento cirúrgico para olhar os órgãos dentro do abdômen para checar sinais de doença. Pequenas incisões (cortes) são feitas na parede do abdômen e um laparoscópio (um tubo fino e iluminado) é inserido em uma das incisões. Outros instrumentos podem ser inseridos através das incisões para realizar procedimentos, como a remoção de amostras de tecidos para pesquisas. Pode também, em alguns casos, realizar-se parte da cirurgia para tratamento por esse método.
– PET Scan (Tomografia por emissão de pósitrons scan): é um exame que combina a tomografia computadorizada e uma espécie de cintilografia. É utilizada uma substância radioativa (fluordesoxiglicose – FDG), que é injetada por uma veia e é mais absorvida por células tumorais, fazendo com que o câncer possa ser diagnosticado ou analisado com grande precisão.
Tratamento do câncer de estômago
Três tipos de tratamento são utilizados para o câncer de estomago. São eles:
– Cirurgia: é o tratamento mais comum para todos os estágios do câncer de estômago. Os seguintes tipos de cirurgia podem ser utilizados:
• Gastrectomia subtotal: remoção de parte do estômago que contém o câncer, linfonodos próximos, tecidos ou órgãos que possam estar acometidos pelo tumor.
• Gastrectomia total: remoção de todo o estômago, os linfonodos próximos, parte do esôfago, duodeno e outros tecidos próximos ao tumor. O baço pode ser removido. O esôfago é ligado ao intestino delgado para que o paciente possa continuar a comer e engolir. Se o tumor está obstruindo o estômago, mas o câncer não pode ser completamente removido por cirurgia, pode se realizar a colocação de uma prótese (um tubo fino e expansível), realizado através de endoscopia, a fim de manter uma passagem para o alimento.
– Radioterapia: a radioterapia é um tratamento contra o câncer que utiliza tipos de radiação para matar células cancerígenas ou impedi-las de crescer. Existem dois tipos de radioterapia: a terapia de radiação externa – a mais comum, que utiliza uma máquina para enviar radiação para o câncer; e a terapia de radiação interna (braquiterapia) – na qual a substância radioativa é colocada diretamente em contato com o tecido tumoral.
– Quimioterapia: um tratamento de câncer que usa medicamentos (remédios) para parar o crescimento das células cancerosas, matá-las ou impedi-las de se dividir. Quando a quimioterapia é tomada via oral ou injetada numa veia ou músculo, os remédios entram na corrente sanguínea e podem atingir as células cancerosas por todo o corpo (quimioterapia sistêmica). Quando a quimioterapia é colocada diretamente na coluna vertebral, um órgão ou uma cavidade do corpo, como o abdômen, as drogas afetam principalmente as células do câncer nessas áreas (quimioterapia regional). A forma como a quimioterapia é dada depende do tipo e estágio do câncer a ser tratado.

A quimioterapia é um dos principais tipos de tratamento no combate ao câncer. Trata-se de uma terapia que utiliza medicamentos para destruir as células doentes que formam um tumor. Estes remédios se misturam com o sangue e são levados a todas as partes do corpo, destruindo as células ruins que estão formando a doença e impedindo, também, que elas se espalhem pelo organismo.
Para esclarecer as principais dúvidas sobre a quimioterapia e sua importância na luta contra o câncer, eliminar os mitos envolvendo esse tipo de tratamento e ainda saber mais informações sobre seus efeitos colaterais, o Hospital de Amor traz uma entrevista exclusiva com o oncologista clínico da instituição, Dr. Luís Eduardo Zucca. Confira!
1) Qual é o principal objetivo da quimioterapia no tratamento de câncer?
R.: Existem 4 tipos de tratamento com quimioterapia:
• A quimioterapia neoadjuvante: esse tipo de quimioterapia é utilizado antes de um tratamento curativo para um tumor localizado. Geralmente, faz-se sessões de quimioterapia para tentar a redução do tumor e, assim, no tratamento curativo (seja ele com radioterapia ou cirurgia), o resultado ser mais efetivo e eficaz. Dessa forma, há menos riscos do desenvolvimento de comorbidades (surgimento de outras doenças em simultâneo) para o paciente.
• A quimioterapia adjuvante: utilizada após um tratamento curativo (seja ele em cirurgia ou radioterapia), tem o objetivo de diminuir e tentar matar todas as micrometástases (células cancerígenas se multiplicam num local distante para formar pequenos tumores) que possivelmente possam ter ficado no corpo, diminuindo assim as chances do câncer voltar.
• A quimioterapia paliativa: como o próprio nome diz, serve para paliar (amenizar) os sintomas dos pacientes. Podem ser pacientes que estejam com dor (proporcionando a melhora a deles com o uso da quimioterapia) e, por última instância, para melhorar a sobrevida com medicamentos quimioterápicos paliativos nos casos de pacientes com tumores metastáticos (quando o câncer se espalha além do local de origem para outras partes do corpo).
• A quimioterapia concomitante à radioterapia: nestes casos, a quimioterapia serve como um veículo para aumentar a potência da radioterapia.
2) Ela é indicada para quais tipos de tumores?
R.: A quimioterapia (seja ela neoadjuvante, adjuvante, paliativa ou concomitante à radioterapia) é indicada para a maioria dos tumores malignos.
3) Como é realizado o procedimento?
R.: Existem, basicamente, 2 tipos principais de procedimentos quimioterápicos: a quimioterapia intravenosa (pela veia), na qual o paciente é puncionado por uma veia periférica ou mesmo por um port-a-cath (dispositivo colocado pelo cirurgião dentro de uma veia mais calibrosa – aquelas com maior dilatação – no corpo do paciente); e a quimioterapia injetável, que é feita em ambientes preparados para receber a quimioterapia com um enfermeiro especializado. Geralmente, os pacientes ficam de 30 minutos até 6 horas fazendo quimioterapia intravenosa. Além disso, existem também as quimioterapias administradas por via oral, nas quais o paciente leva para casa os comprimidos orais e ingere de acordo com o esquema quimioterápico que o médico fornece para ele.
4) Existe mais de um tipo de quimioterapia?
R.: Existem vários tipos de quimioterapias, desde as específicas para certo tipo de tumor, até a quimioterapia que nós tratamos para uma variedade de tumores.
5) Existem efeitos colaterais na utilização da quimioterapia? Quais?
R.: As quimioterapias têm alguns efeitos colaterais manejáveis. Dependendo do esquema de quimioterapia que o paciente recebe, podem ocasionar náuseas, vômitos, cansaço, fadiga e baixa energia. A questão central, também dependendo do esquema de quimioterapia, é que geralmente os tratamentos quimioterápicos não matam apenas as células ruins, atingindo células boas que se multiplicam rapidamente (como cabelo e unha). Então, alguns esquemas quimioterápicos podem ocasionar a queda de cabelo e algumas alterações, mas também as células de defesa do nosso corpo. Dessa forma, em alguns casos, elas podem deixar o nosso corpo mais vulnerável a infecções.
6) Quando esses efeitos aparecem, o que é preciso fazer?
R.: Quando qualquer um desses efeitos aparecer é necessário procurar o seu médico e procurar o hospital. Por exemplo, para os pacientes que estão fazendo quimioterapia e têm febre, a primeira recomendação indicada é a procura do Hospital para passar pela avaliação do médico, pois como a quimioterapia também mata as células boas, o corpo fica vulnerável à infecção. Uma vez que o paciente tenha infecção e células de defesa baixa, nós, médicos, precisamos iniciar antibióticos e terapias o mais rápido possível. Mas, existem outros efeitos colaterais também manejáveis, como náuseas, vômitos, fadigas, inclusive queda de cabelo.
7) Qual é o tempo mínimo e qual é o tempo máximo de duração da quimioterapia?
R.: Existem vários tempos de quimioterapia, desde as que duram 15 minutos, como a blaumicina; aquelas que podem durar o dia inteiro, como a cisplatina; ou até a quimioterapia que o paciente vai para casa com um dispositivo e a quimioterapia fica correndo durante 48 horas dentro do seu organismo.
8) O paciente que é submetido a esse tipo de tratamento pode seguir sua rotina de atividades/trabalho normalmente?
R.: Dependendo do tipo de quimioterapia e do esquema quimioterápico, sim, é possível viver normalmente, inclusive trabalhando, estudando, fazendo as atividades diárias. Isso porque, hoje em dia, a maioria dos efeitos colaterais é bastante controlável, porém, sempre é necessário respeitar o próprio corpo.
9) Em média, quais são os custos da quimioterapia?
R.: O custo da quimioterapia também é variável, desde quimioterapias mais baratas, até aquelas que custam de 20 a 30 mil reais por mês.
Desde 2015, o Hospital de Amor conta com um programa de rastreamento para a detecção precoce do câncer colorretal – aquele que acomete o trato digestivo (intestino grosso e reto). De lá para cá, já foram alcançadas 12.723 pessoas, sendo 48 pacientes diagnosticados com esse tipo de tumor.
Conheça mais sobre o câncer colorretal, seus sintomas e saiba como se prevenir.
O que é câncer colorretal?
Os cânceres colorretais são aqueles que acometem o trato digestivo (intestino grosso e reto). Esses tumores são considerados mais passíveis de prevenção, pois a evolução natural deles é bem conhecida pela medicina: eles começam com lesões precursoras, ou seja, lesões pré-malignas (também conhecidas como pólipos) que são detectáveis e que podem ser removidas. Com essas medidas, é possível interromper a progressão da doença. Geralmente, as chamadas ‘lesões precursoras’ não apresentam sintomas (como sangramentos ou dores abdominais), por isso, para identificá-las, é necessário submeter o indivíduo a um rastreamento para prevenir a evolução da doença.
O que são pólipos?
São tumores benignos, parecidos com verrugas, que se desenvolvem na parte interna do cólon e reto. Cerca de 60% dos pólipos do intestino são adenomas e podem apresentar potencial para se tornarem tumores malignos. É importante que o diagnóstico e o tratamento sejam feitos precocemente, principalmente após os 50 anos e em caso de história de câncer colorretal na família.
Quais são os sinais e sintomas do câncer colorretal?
Os principais sintomas da doença são: mudança do hábito intestinal, isto é, constipação ou diarreia sem associação com o alimento ingerido; anemia sem causa aparente, principalmente em pessoas com idade acima de 50 anos; fraqueza; desconforto abdominal (com gases ou cólicas); emagrecimento intenso e inexplicável; sangramento pelo reto; e sensação de evacuação incompleta.
Qualquer pessoa que apresentar um desses sintomas deve procurar o médico, principalmente se houver sangramento anal, para que os exames clínicos necessários sejam realizados. Entre os exames estão: realização do toque retal e do exame de colonoscopia (procedimento de vídeo utilizado para visualizar o interior do intestino grosso e a parte final do intestino delgado).
Quais os fatores de risco para o desenvolvimento da doença?
Uma alimentação rica em carnes vermelhas, carnes processadas (como salsichas e mortadelas) e gorduras, além da ausência de atividade física regularmente (como o sedentarismo), ingestão abusiva de álcool, tabagismo, sobrepeso e obesidade, são alguns fatores externos que podem contribuir para o desenvolvimento da doença.
Pessoas com idade superior a 50 anos, ou que já tenham tido pólipos ou doença inflamatória intestinal, ou que tenham histórico de ocorrência de câncer colorretal em familiares, devem ficar atentas aos sinais.
Como se prevenir deste tipo de câncer?
Prevenir significa evitar os fatores que estão relacionados com o desenvolvimento de câncer colorretal. Adotar uma alimentação rica em frutas, verduras e vegetais, evitar o consumo de carnes vermelhas e embutidos, praticar exercício físico, evitar a obesidade, evitar o consumo de bebidas alcoólicas e cigarros, são importantes atitudes de prevenção. Os alimentos ricos em fibras protegem o intestino, pois facilitam a evacuação, aceleram o trânsito intestinal e diminuem o tempo de contato das substâncias carcinogênicas (que levam à formação do câncer) com a parede do intestino.
Refletir sobre os hábitos e estilo de vida é sempre uma forma de se prevenir de qualquer tipo de câncer e conquistar uma vida mais saudável. Confira algumas dicas:
– Praticar exercícios físicos regulares;
– Não fumar;
– Não ingerir bebidas alcóolicas;
– Não ingerir alimentos defumados, enlatados ou embutidos;
– Não ingerir alimentos com corantes e/ou conservantes;
– Se diagnosticado, remover pólipos através do exame de colonoscopia;
– Ingerir alimentos ricos em vitaminas C e E.
Porém, apesar de todos esses cuidados, também é necessário participar dos programas de rastreamento, pois essas medidas não são 100% eficazes. Existem dois exames que podem ser utilizados para rastrear esse tipo de tumor, sendo eles: o teste de imunoquímica fecal (conhecido também como teste FIT ou exame de sangue oculto nas fezes) e a colonoscopia (que é um exame de vídeo para visualizar o interior do intestino grosso e a parte final do intestino delgado). Recomenda-se iniciar o rastreamento a partir dos 50 anos, mas, cabe ao médico indicar qual é a melhor opção de procedimento para cada paciente.
Como é o teste FIT?
Também conhecido como exame de sangue oculto nas fezes, o teste FIT é indicado para um público bem específico: homens e mulheres que tenham entre 50 e 65 anos, que não tenham feito nenhum exame de colonoscopia ou de retossigmoidoscopia nos últimos 5 anos, não tenham nenhum histórico de doença inflamatória intestinal e de pólipos colorretais.
São necessárias três amostras de fezes consecutivas. Alguns dias antes do exame, alguns tipos de alimentos devem ser evitados. Além disso, medicamentos como AAS e anti-inflamatórios não devem ser tomados 7 dias antes do exame, e frutas cítricas e carne vermelha não devem ser consumidas três dias antes do procedimento. Se o resultado para o sangue oculto for positivo, será necessário realizar o exame de colonoscopia.
Como é a colonoscopia?
É um exame realizado por um aparelho de fibra ótica, longo (180 cm) e flexível, que é introduzido através do ânus e permite a visualização completa do reto e do cólon. Essa visualização ocorre por uma câmera inserida na extremidade do colonoscópio, cuja imagem é enviada para um monitor, permitindo assim, a análise simultânea do interior do cólon. O equipamento também permite a inserção de outros instrumentos especiais para a remoção de possíveis pólipos ou biópsias. O exame é feito sob sedação e analgesia, permitindo que o médico examine detalhadamente o cólon. Os riscos do procedimento são pequenos e estão vinculados ao sangramento depois da retirada de pólipos, biópsias e perfuração intestinal.
Como é tratamento para o câncer colorretal?
O tratamento para os tumores iniciais, geralmente, é menos agressivo, com a retirada de pólipos e lesões através da colonoscopia ou das cirurgias com ressecções locais dos tumores.
Nos tumores maiores do cólon, há a necessidade de cirurgia (convencional, laparoscópica ou robótica).
Nos tumores do reto, pode ser necessário realizar procedimentos radioterápicos e quimioterápicos antes da cirurgia.
Em resumo, o tratamento para o câncer colorretal envolve radioterapia, quimioterapia e/ou cirurgia, dependendo do local, do tamanho e da extensão da doença no cólon ou em outros órgãos (no caso de metástases – aparecimento do tumor em outros órgãos, como fígado ou pulmão, por exemplo). Quanto mais precocemente a doença for diagnosticada, menor a agressividade e o tempo de tratamento, proporcionando melhor qualidade de vida ao paciente.



Os milhares de pacientes que realizam tratamento no Hospital de Amor Barretos agora contam com uma nova alternativa de medicação para os tratamentos de cânceres de pulmão e melanoma (tipo mais grave de câncer de pele) em estágios avançados. Graças à parceria firmada com a farmacêutica MSD, a instituição poderá oferecer aos pacientes do Sistema Único de Saúde (SUS) o tratamento com a terapia anti-PD-1, conhecida como pembrolizumabe (Keytruda). O Hospital de Amor é a primeira entidade de saúde pública no Brasil a oferecer a imunoterapia.
A assinatura do termo aconteceu na última segunda-feira, dia 3 de setembro, reunindo médicos, o presidente do Hospital, Henrique Prata, e o diretor-geral do Centro Oncológico “Antônio Ermírio de Moraes” – Beneficência Portuguesa, de São Paulo, e membro do comitê de direção do Centro Oncológico do Hospital Israelita Albert Einstein, Dr. Antônio Buzaid.
De acordo com Buzaid, o tratamento imunoterápico é uma nova alternativa para a quimioterapia, além de possuir efeitos colaterais menores. “Quando aplicamos o Anti-PD-1, estimulamos uma sobrevida no paciente. Por isso, é tão importante investir em pesquisas clínicas para aumentar a receita da instituição e melhorar o tratamento básico. Para nós, o Hospital de Amor é um motivo de muito orgulho”, afirmou.
Para a diretora médica de oncologia da MSD Brasil, Dra. Márcia Datz Abadi, “o pembrolizumabe representa um avanço importante no tratamento do câncer e é um orgulho poder oferecer essa inovação aos pacientes do SUS. Nos sentimos honrados pela parceria e pioneirismo do Hospital de Amor”.
Após essa conquista, o HA poderá facilitar o acesso ao medicamento, acelerar o tratamento e as chances de cura e sobrevida dos pacientes. A estimativa é de que em duas semanas essa alternativa já esteja sendo aplicada na instituição. Segundo Henrique Prata, a assinatura do convênio representa um marco histórico nos mais de 50 anos de trajetória do Hospital e também para a oncologia brasileira. “Todas as pessoas têm direito de ter um tratamento digno. Portanto, temos muito o que comemorar com essa conquista”, declarou.

Câncer de Pulmão
O câncer de pulmão é considerado o mais comum e letal entre todos os tumores malignos. A estimativa do Instituto Nacional do Câncer (INCA) para este ano é de que 30 mil novos casos sejam diagnosticados no Brasil, sendo o de células não pequenas o mais comum – correspondente a 85% de todos os casos. Estimativas globais apontam que apenas 1% dos pacientes com câncer de pulmão avançado estão vivos, cinco anos após o diagnóstico.
Em junho, o Brasil se tornou o primeiro país do mundo a aprovar, baseado em um estudo de fase 3, o uso combinado de pembrolizumabe e quimioterapia para tratamento de pacientes com câncer de pulmão de células não pequenas (CPNPC) em estágio avançado ou metastático. De acordo com o estudo KEYNOTE-189, publicado no New England Journal of Medicine, o uso de pembrolizumabe associado à quimioterapia (pemetrexede e cisplatina ou carboplatina), quando utilizado em primeira linha de tratamento, reduz em 51% o risco de morte.
Para o oncologista clínico do HA, Dr. Pedro de Marchi, poder oferecer esse medicamento gratuitamente aos pacientes é um motivo de grande alegria. “Sem dúvida, estamos falando de um marco na história do Brasil. Com essa nova alternativa, a sobrevida é de 8 meses a 3 anos”, ressaltou.
O oncologista explica ainda que o Hospital de Amor recebe cerca de 600 novos pacientes com câncer de pulmão, por ano. Desses, 450 irão precisar de tratamento sistêmico. Entre eles, 360 possuem doença metastática. Desses, 320 não têm mutações. “Isso quer dizer que, desses 320 pacientes, 17% apresenta PD-L1 maior que 50% e seriam candidatos a esse tipo de tratamento, o que resultaria em, aproximadamente, 54 pacientes novos por ano”, finalizou Dr. Pedro de Marchi.
Câncer Melanoma
O melanoma é caracterizado pelo crescimento descontrolado de células que compõem a pele. A incidência deste tipo de câncer tem aumentado nas últimas quatro décadas. Só o Brasil registra, anualmente, cerca de 5.500 novos casos da doença e, aproximadamente, 1.547 óbitos, segundo o INCA. Esse tipo de câncer é considerado o mais comum entre jovens adultos, mas também pode ser diagnosticado em crianças, adolescentes e idosos.
De acordo com o estudo Keynote-001, em 655 pacientes com melanoma metastático, 34% de todos eles e 41% dos que não haviam tido qualquer tratamento prévio, permanecem vivos após 5 anos do uso de pembrolizumabe, em uma doença em que a quimioterapia oferecia apenas poucos meses de sobrevida. Já o estudo KEYNOTE-006 mostrou que 42% dos pacientes tratados com pembrolizumabe estavam vivos após quatro anos de diagnóstico.
“É trágico saber que somente pacientes que possuem convênios ou acesso aos atendimentos privados, conseguem ter acesso a esse tipo de tratamento. Agora, pela primeira vez, os pacientes do SUS, atendidos no Hospital de Amor, poderão contar com uma medicação inovadora. É uma luz de esperança para que, em pouco tempo, mais pacientes possam conseguir esta e todas as outras medicações que ainda não estão disponíveis gratuitamente”, declarou o oncologista clínico do HA, Dr. Sérgio Serrano.
O medicamento
O medicamento (pembrolizumabe) já pode ser utilizado no Brasil para o tratamento em primeira linha de melanoma avançado para pacientes com câncer de pulmão avançado, do tipo CPCNP, com expressão elevada ou moderada do biomarcador PD-L1 no tumor (expressão ≥50% ou 1%<49%) e tratamento de câncer urotelial (o mais comum é o câncer de bexiga). Ele também foi aprovado este ano para tratamento de câncer gástrico (o mais comum é o de estômago), após falha de duas terapias prévias.
A imunoterapia anti-PD-1 da MSD está sendo avaliada para mais de 30 tipos de tumores em 790 estudos clínicos. No Brasil, o medicamento está sendo pesquisado em mais de 29 ensaios clínicos, com cerca de 232 instituições envolvidas e mais de 500 pacientes em tratamento.

Publicado em 06 de set de 2018 | Artigos, Destaques, Institucional, Ensino e Pesquisa, Diagnóstico e Tratamento

Oferecer tratamento oncológico de qualidade e de maneira humanizada é rotina no Hospital de Amor! Para cada diagnóstico de câncer, há um protocolo diferente e personalizado de intervenção, mas em todos eles, há humanização para garantir o bem-estar do paciente. E dentre tantas possibilidades de tratamento, a quimioterapia (apesar de temida por conta de seus efeitos colaterais) ainda é um dos mais eficazes para diversos tipos de tumor.
Trata-se de um procedimento em que se utilizam medicamentos – que se misturam com o sangue e são levados a todas as partes do corpo – para destruir as células doentes que estão formando o tumor, impedindo também que se espalhem. Quando esta aplicação é intravenosa, ou seja, aplicada na veia ou por meio de cateter, ela pode causar alguns desconfortos nos pacientes que a recebem. E é aí que, mais uma vez, o HA se destaca!
Projeto inovador
Com o objetivo de minimizar os riscos de cardiotoxicidade e os efeitos colaterais induzidos pela quimioterapia, a equipe do departamento de fisioterapia da instituição, por meio do ‘Programa de Fisioterapia na Atenção ao Câncer’, desenvolveu um projeto de pesquisa inovador, que busca elaborar um plano de exercícios de baixa à média intensidade para realização durante a infusão de quimioterapia.
O estudo, idealizado pela coordenadora do departamento de fisioterapia do Hospital de Amo, Dra. Carla Elaine Laurienzo da Cunha Andrade, junto a fisioterapeuta, Simara Cristina Pereira da Silva, e a residente de fisioterapia, Brenda Taynara Macedo da Costa, foi implementado em outubro deste ano na instituição e já atendeu mais de 20 pacientes.
“Com este protocolo poderemos comprovar que a realização de exercícios físicos (de baixa à média intensidade), durante a infusão de quimioterapia, promove a melhora da funcionalidade, fadiga, neuropatia e, principalmente, o bem-estar dos pacientes do estudo, quando comparados aos pacientes que não realizam nenhuma atividade física durante o momento da infusão”, explica Dra. Carla.
Neste primeiro momento, o estudo está sendo realizado em mulheres com diagnóstico de câncer de mama, que tenham entre 18 e 60 anos e aceitem participar do protocolo. Porém, a prática de aliar quimioterapia a exercício físico é indicada para todos os tipos de câncer, podendo beneficiar todos os pacientes do HA que passam por tratamento quimioterápico.
“Há evidências na literatura que indicam que o exercício realizado durante a infusão de quimioterapia, promove aumento da perfusão que pode melhorar a administração do medicamento e atenuar alguns efeitos colaterais dele. Então, além dos benefícios relacionados a própria quimioterapia, o projeto poderá influenciar também no hábito da prática de atividade física, promovendo uma maior adesão e entendimento para os pacientes sobre a importância de se manterem ativos durante o tratamento oncológico e as vantagens dos exercícios para sua saúde física e emocional”, afirma a coordenadora.
Como funciona?
A paciente que se encaixa em todos os requisitos exigidos pelo estudo e aceita participar do projeto, é direcionada para o Centro Infusional do HA, em Barretos (SP), nas salas comuns de infusão. Durante a sessão de quimioterapia, uma fisioterapeuta com especialização em oncologia leva o ‘kit de exercícios’, inclusive uma minibicicleta ergométrica e um fone de ouvido, e inicia as atividades. “Para a realização dos exercícios, a paciente escolhe a playlist que desejam ouvir durante o procedimento e escuta a seleção de músicas em fones de ouvido. Além da humanização, esse tipo de intervenção também é uma forma de diminuir o tédio durante as horas de infusão em que as pacientes ficam nas poltronas, tornando este momento um pouco mais leve na jornada do seu tratamento”, declarou Dra. Carla.
A paciente Fernanda Barbosa, de 43 anos, consegue identificar todos esses benefícios! Em tratamento no HA contra um câncer de mama, a mineira de Araxá, que sempre praticou atividades físicas e necessitou parar por conta dos efeitos colaterais decorrentes dos procedimentos, sentiu diferença pós receber a quimioterapia associada aos exercícios. “Em poucos minutos realizando as atividades, senti que minha ansiedade foi embora, eu fiquei muito mais disposta e a tremedeira melhorou. Vale muito a pena”, conta.
De acordo com a coordenadora do departamento de fisioterapia do HA, ainda são poucas as instituições oncológicas do país que realizam este tipo procedimento. “Estudos nessa área também são escassos, ou seja, o Hospital de Amor está sendo pioneiro e inovador!”, finalizou.


Em 2004, o cofundador da Apple, Steve Jobs, foi diagnosticado com câncer de pâncreas. Oito anos depois, com o tumor em estado metastático (ou seja, espalhado por outros órgãos) e algumas complicações, ele faleceu. De acordo com o Instituto Nacional do Câncer (INCA), a doença representa 2% do total de casos diagnosticados no país e 4% das mortes. Isso porque possui difícil detecção e por ter comportamento agressivo, o que limita as opções de tratamento.
No Brasil – sem contar os tumores de pele não melanoma – o câncer de pâncreas ocupa a 14ª posição entre os tipos de câncer mais frequentes, sendo considerado por especialistas como uma das formas mais letais de tumor maligno (ele costuma matar 95% dos pacientes em cinco anos). Em números absolutos, o INCA calcula que em 2020 essa doença matou 5.882 homens e 6.011 mulheres, tornando-se o sétimo tumor mais mortal para eles e o quinto para elas.
Diversas personalidades foram vítimas do câncer de pâncreas (ainda pouco divulgado), entre elas o ator americano Patrick Swayze, o tenor italiano Luciano Pavarotti e o ator brasileiro Raul Cortez. Afinal: quem nunca teve um parente ou amigo próximo com câncer de pâncreas?
O Hospital de Amor conversou com coordenador do departamento de cirurgia digestiva alta da instituição, Dr. Fernando Ernesto Cruz Felippe, e preparou uma matéria especial sobre o tema, esclarecendo as principais dúvidas sobre a doença, suas formas de prevenção, e sinais e sintomas.

Assim como acontece em outros meses do ano, setembro também conta com uma importante campanha de conscientização: a do retinoblastoma – o câncer dos olhos mais comum na infância. O “Dia Nacional de Conscientização e Incentivo ao Diagnóstico Precoce do Retinoblastoma”, celebrado em 18 de setembro, tem o objetivo de alertar a sociedade sobre a importância da detecção precoce da doença, fator indispensável para garantir bons resultados no tratamento.

A iniciativa ganhou força e uma visibilidade ainda maior! Após o casal Tiago Leifert e Diana Garbin revelarem (no ano de 2022) que sua filha, Lua (na época com apenas 1 ano e 3 meses), tinha sido diagnosticada com um tipo raro de câncer na retina, o retinoblastoma bilateral, os jornalistas assumiram a missão de alertar outros pais para os perigos da doença, enquanto a filha segue em tratamento.
Neste ano, o Conselho Federal de Medicina (CFM), a Associação Médica Brasileira (AMB), o Conselho Brasileiro de Oftalmologia (CBO) e a Sociedade Brasileira de Pediatria (SBP), além de outras entidades médicas, promoveram a mobilização “De olho nos olhinhos”. E o Hospital de Amor – referência em tratamento oncológico gratuito de excelência, com o maior serviço de prevenção de câncer do país – é uma das instituições que apoia esta grande ação.
Confira!
– O que é retinoblastoma?
R.: O retinoblastoma é o câncer dos olhos mais comum na infância e representa cerca de 2,5 a 4% de todas as neoplasias pediátricas.
– Qual é a incidência deste câncer?
R.: O retinoblastoma é um tumor raro, com cerca de 400 casos novos por ano no Brasil. Trata-se de uma doença da primeira infância, com maior incidência nas crianças abaixo de 5 anos de vida. De acordo com o Ministério da Saúde, a maioria dos casos – entre 60% e 75% – é unilateral (quando afeta um olho). Destes, 85% são esporádicos, e os demais são casos hereditários. Já o bilateral (quando os dois olhos são afetados), são quase sempre casos hereditários.
– Quais são os principais sintomas de retinoblastoma?
Outros sintomas que podem aparecer são: vermelhidão, deformação do globo ocular, baixa visão, conjuntivite, inflamações e dor ocular.
– Quais sãos os perigos da doença quando se trata de perder a visão?
Nos casos bilaterais, frequentemente apenas um dos olhos tem uma doença avançada, que evolui com sequelas visuais mais importantes. Nesses casos, o olho com doença menos avançada costuma ter um ótimo resultado visual e permite que a criança realize a maioria das atividades diárias normalmente, inclusive participar de esportes e dirigir na vida adulta.
– Existe prevenção ou cura para a doença?
Todas as crianças devem passar por uma primeira avaliação oftalmológica completa, que inclua o exame de fundo de olho com a pupila dilatada, entre 6 meses e 1 ano de vida. Por ser uma doença que frequentemente envolve mutações genéticas herdadas em famílias com casos de retinoblastoma, as crianças devem ser avaliadas e acompanhadas desde o nascimento.
– Quais são os tipos de tratamento para o retinoblastoma?
Já em casos de doença avançada, pode ser necessário fazer a remoção do globo ocular afetado, com reconstrução da órbita e adaptação de uma prótese para um bom resultado estético.
– E como funciona a quimioterapia intra-arterial?
R.: A quimioterapia intra-arterial é um procedimento multidisciplinar de alta complexidade. Envolve o radiologista intervencionista, oncologista pediátrico, anestesista, oftalmologista, farmacêutico e uma grande equipe de suporte. Nela, um micro cateter é introduzido desde a artéria femoral até a artéria oftálmica, responsável pela nutrição do globo ocular.
– Qual é o grande diferencial deste tipo de tratamento em relação as quimioterapias convencionais?
Mas é importante lembrar que: o tratamento do retinoblastoma é feito de forma personalizada, ou seja, cada caso é um caso e necessita de avaliação médica.
– O Hospital de Amor oferece, gratuitamente, o que há de mais avançado aos pacientes, inclusive nos tratamentos de retinoblastoma?

Ação “De olho nos olhinhos”
Além de publicações semanais nos perfis oficiais da instituição durante todo o mês de setembro, trazendo conteúdos informativos sobre o tema, o Hospital de Amor também realiza uma ação especial para a população de Barretos (SP) e região. Nos dias 15 e 16/9, uma equipe de profissionais da unidade infantojuvenil do HA estará no North Shopping Barretos alertando, informando e conscientizando as pessoas para a importância do diagnóstico precoce do retinoblastoma. Cartazes e cartilhas serão entregues em todas as unidades de saúde administradas pela rede HA. Prestigie, apoie esta campanha e nos ajude nessa missão!
E se você é pai, mãe, avó, professora ou convive com crianças, fique atento aos sintomas de alerta para o retinoblastoma. Com a presença de qualquer um dos sinais, é imprescindível levar os pequenos para uma avaliação médica.
Independente da situação, o exame oftalmológico deve ser feito mesmo sem qualquer suspeita de comprometimento visual. Ao nascer: teste do olhinho; entre 6 meses e 1 ano de vida: primeiro exame oftalmológico completo; em torno de 3 anos de idade: segundo exame oftalmológico completo; entre 5 e 6 anos: novo exame oftalmológico; a partir daí: o exame oftalmológico terá a frequência dependendo da saúde visual da criança e o histórico familiar.

Desfilar na passarela, atrair muitos olhares, brilhar e ser protagonista dos holofotes faz parte do sonho de muitas jovens. Com a Ingrid Assis não é diferente! Natural do Amapá (AP), a adolescente de 15 anos parece ser uma jovem comum, mas apenas parece, pois tem algo de realeza nesta história de superação. Cheia de sonhos, desenvolta e muito vaidosa, ela precisou se mudar para Barretos (SP) para dar início ao seu tratamento de osteossarcoma na tíbia direita, em março de 2022.
Elenita de Oliveira Silva, mãe da Ingrid e técnica em enfermagem, revela que a filha começou a apresentar dores no joelho. Após perceber que havia algo de errado com a jovem, ela então a levou para fazer exames e investigar o caso, foi quando receberam o diagnóstico de um tumor. Ao não ter recursos para um bom tratamento na sua cidade de origem e após receber o apoio de um parente que atua como médico ortopedista em Sorocaba (SP), e que conhece o HA, ele a ajudou nos tramites; foi quando a família da jovem decidiu se mudar para o interior de São Paulo.

“Eu conheci o HA por meio de um primo que me falou que o Hospital de Amor é um ótimo hospital e que tem um dos melhores tratamentos do Brasil. Vim para o estado de São Paulo ano passado e, na época, eu ainda não tinha certeza de que eu estava com câncer”, conta a jovem. Inicialmente, a esperança da família da garota é de que o tumor fosse benigno, mas infelizmente, a biópsia resultou em algo oposto ao desejo deles.“Na minha cabeça, era vir a Barretos, tirar o tumor e voltar para casa, achei que seria algo rápido, nada que mudasse a minha vida”, revela a adolescente. No entanto, após os exames foi constatado que o tumor era maligno e deste modo, a garota precisou passar pelo tratamento durante 31 semanas.
Ingrid explica que precisou fazer quimioterapia e que sofreu com a queda de cabelo e com tudo que os procedimentos oncológicos trazem aos pacientes. No meio desta jornada, a jovem precisou realizar uma operação na unidade infantojuvenil do HA. Ela fez a cirurgia, porém, devido à uma infecção, houve a necessidade da amputação da perna dela. “As pessoas aqui do hospital são muito acolhedoras e os médicos são atenciosos. No dia da minha amputação, meu pai me disse que o meu cirurgião quase chorou pela minha situação. Me sinto muito abraçada no Hospital de Amor”, relata a macapaense, sempre com um belo sorriso no rosto.
“Hoje ela é uma vencedora, graças a Deus e a este hospital. Eu estou muito feliz de ver como ela está e com a reabilitação dela. A fisioterapia aqui é maravilhosa. São processos e fases que ela tem vivido. Participar do concurso do rodeio trouxe mais ânimo e alegria para ela. Eu só tenho que agradecer a este local que nos acolheu tão bem”, conta Elenita ao ver a evolução de ver sua filha com a prótese.

Recomeço de uma nova história
Em abril deste ano, a jovem iniciou seu processo de reabilitação no HA, foi quando ela recebeu sua primeira prótese para poder voltar andar normalmente. A paciente conta com o apoio de uma equipe multiprofissional e da ‘Tia Deise’, como é carinhosamente conhecida a fisioterapeuta do HA, Deiseane Bonatelli. “A gente procura oferecer todo suporte necessário para que ela tenha uma maior independência na vida dela, para que ela possa fazer todas as necessidades possíveis”, conta Deise.
A profissional também revela a alegria de poder ajudar a garota a participar de um grande desafio. “Eu me sinto muito feliz de ver ela rainha do Rodeio pela Vida. Quando ela disse que iria entrar no concurso, eu combinei com ela para voltar aqui e treinar para andar bem bonito no dia da competição. Ela voltou, nós treinamos e ela venceu. Eu me sinto muito feliz por ela”, explica com os olhos marejados a ‘Tia’ que é muito querida por todos os pacientes, desde crianças, adultos e idosos.
Quando perguntada sobre o processo de aprendizado de voltar a andar, Ingrid, de imediato responde com um lindo sorriso no rosto: “Não tem limite. O seu limite é você mesmo, mas a prótese não te limita. Eu conheço um homem, pela internet, que escala com prótese”.
Mas engana-se quem pensa que Ingrid não tinha pisado em solo barretense antes de seu tratamento. “Eu vim a Barretos em 2019, para participar de um evento da igreja no qual congrego e nunca imaginei que eu voltaria para cá por outro motivo. É difícil, mas quando a gente entrega tudo nas mãos de Deus, tudo fica mais leve. Eu não sei até hoje porque eu perdi a minha perna, mas eu confio em Deus e sei que tudo tem um propósito”.
A competição e seu reinado
No início do ano, o HA abriu as inscrições para a 3ª edição do Rodeio Pela Vida 2023 – evento que acontece em Barretos (SP) e é organizado pela instituição, com renda 100% em prol do Hospital de Amor. Incentivada pela ‘Tia Lili’, uma das organizadoras do evento ‘Fadas Madrinhas’, Ingrid tomou coragem e fez sua inscrição.
Inicialmente, ela disse acreditar que no máximo ficaria no 3º lugar, pois o páreo parecia duro. Ao ser revelado seu nome como a rainha do rodeio, ela não escondeu a surpresa e ficou em êxtase. “Estou muito feliz de ter sido eleita a rainha, se puder, eu quero muito conhecer o padre Fábio de Mello e dar um abraço nele”, explica a garota entusiasmada.
Ao lado de Ingrid, o concurso elegeu a princesa, Jamily Yasmin Peres do Nascimento, e a madrinha Raquel Galvão de Oliveira. A 3ª edição do “Rodeio Pela Vida” teve início no dia 7 de junho e termina no dia 11 de junho, no Recinto Paulo de Lima Correa. Quando questionada sobre um conselho que a rainha daria para pessoas que estão passando pelo mesmo enfrentamento que recentemente ela concluiu, ela não titubeia e logo responde: “Se você está passando por um problema, confie em Deus que vai dar tudo certo.”


Quando começou a sentir dores na região das costas, José Benedito Costa, de 61 anos, não imaginava que o destino lhe proporcionaria uma viagem de cerca de 4 mil quilômetros de distância de sua casa. Atravessar o Brasil não estava em seus planos quando as coisas começaram a sair da rotina.
O roraimense de Boa Vista (RO) viu sua vida mudar completamente ao receber o diagnóstico de câncer em sua cidade de origem. Não bastasse o medo e a ansiedade natural que a doença lhe trazia, também era preciso largar tudo e ir para o interior de São Paulo, para dar início ao seu tratamento. Mas, até chegar ao diagnóstico final, foi uma longa jornada que ele trilhou ao lado de sua esposa, Eliani Amorim, 46 anos, que no mesmo período enfrentava os desafios de um aneurisma que tinha sido detectado em seu cérebro.

O início de uma nova vida
José conta que sentia muita dor no quadril (MarziniClinic), especificamente no cóccix, além de sentir dores ao urinar. “O médico disse que eu tinha uma fistula que precisava operar. Ele já havia realizado mais de 1.200 cirurgias, mas algo como o que eu tinha, ele nunca havia visto”. Durante o procedimento da fistula, o profissional constatou que a situação era mais difícil do que ele pensava.
Ao ficar muito tempo sentado enquanto trabalhava, o ex-técnico em finanças sentia muitas dores. “Descobri que tinha uma fistula que era ocasionada pelo câncer, e foi aí que eu ouvi pela primeira vez a palavra ‘cordoma’. Era necessário fazer uma biopsia para saber qual tipo era”, afirmou. Em abril de 2017, José recebeu o diagnóstico de cordoma (lesão maligna da medula espinhal), em Boa Vista. Seu novo desafio era começar o tratamento contra o câncer.
Por meio da ajuda de uma amiga, foi possível a transferência para o Hospital de Amor, em Barretos (SP). “Vim de voo com o auxílio de um jatinho, direto para o CIA (Centro de Intercorrência Ambulatorial)”, lembra. Após refazer os exames no HA, foi constatado que o ‘cordoma’, na verdade, já estava em metástase.
Após 20 meses, nove ciclos de quimioterapia e uma semana de radioterapia (feitos para conter o crescimento da neoplasia), José realizou a cirurgia para retirar o tumor, em abril de 2019. “Cheguei a ficar dez meses deitado, pois eu já não andava mais, algo que os médicos disseram que nunca mais iria acontecer após o procedimento. Quando cheguei em Barretos, o tumor que inicialmente tinha 5 cm, estava com 10,73 cm”, conta.

De acordo com a sua esposa, o oncologista disse que, após operar, o paciente ficaria um mês no hospital para aprender seu novo estilo de vida, já que ele não iria andar novamente. Ela conta, porém, que de forma surpreendente ele ficou apenas um dia na UTI e, depois de três dias, já estava em casa andando com ajuda do andador.
José revela que os médicos ficaram admirados ao vê-lo caminhar. “Acabei surpreendendo a medicina, porque eles também disseram que eu iria usar a bolsinha de colostomia, além de não caminhar. Eu pedi a Deus para me ajudar e ele me ouviu. Cheguei a criar calo nos joelhos de tanto orar e pedir essa graça”. Após sair do hospital, o paciente precisou usar o andador e em seguida a bengala, mas saiu andando, o que era uma grande conquista para ele, mesmo diante das dores.
“Eu perguntei por que eles não colocaram alguma prótese, pois eles tinham removido meu cóccix todo”, relata José ao lembrar como foi seu diálogo com a equipe médica. Os médicos explicaram que não foi feito este procedimento, pois não era esperado que ele voltasse a andar. Com esse cenário, as dores ao dar seus passos não eram esperadas também.
Posteriormente, a equipe de fisiatras do Centro de Reabilitação do HA identificou que em relação à dor não se podia fazer mais pelo paciente, foi quando entrou em cena a Dra. Margareth Lucca, médica anestesiologista, especializada em dor e em medicina tradicional chinesa, que atua no Hospital de Amor há cinco anos. Nascia assim a esperança de aliviar as sequelas deixadas pela cirurgia.

Arte milenar que combate à dor
A terapia milenar chinesa que consiste na aplicação de agulhas em pontos específicos do corpo do paciente, a fim de tratar enfermidades e promover bem-estar e melhorar a qualidade de vida, é conhecida como acupuntura. Este procedimento é realizado pela médica que diariamente atende, em média, 18 pacientes, dentre eles, adultos e crianças, no centro de reabilitação do HA. “As pessoas chegam irritadas, desanimadas, tristes, sem esperança e com dor. Ao oferecer um trabalho com muito amor e carinho, algo acontece”, revela a Dra. Margareth.
A especialista que iniciou o projeto ‘FADA’ no ambiente de trabalho, explica o nome da ação: Fazendo o Acolhimento da Dor com Aromaterapia – uma outra prática integrativa já reconhecida pelo SUS. Ou seja, por meio de um spray perfumado, ela consegue aromatizar o local, oferecendo bem-estar aos pacientes assim que chegam ao centro. “Como o cheirinho chega até o sistema nervoso central, em um lugar chamado límbico, modifica a reação do corpo, traz um relaxamento, alivia a tensão, a pessoa se sente mais bem acolhida e já muda”, disse a profissional, que também aplica cromoterapia no ambiente, oferendo um tratamento holístico a todos os pacientes que são atendidos por ela.
Ao falar sobre os atendimentos que realiza em José, a médica fica emocionada: “Só de ver o tamanho da cicatriz e conhecer toda história dele, é claro que existe um sofrimento intenso, um bloqueio de ficar restrito pela dor, mas me alegro ao saber que ele jamais perdeu a esperança”.
A terapeuta explica que já realizou infiltrações no paciente em pontos específicos que geram o gatilho da dor. Em seguida, é feito o procedimento da acupuntura. “Este serviço é oferecido via SUS em outros hospitais, mas a maneira com que o Hospital de Amor conduz é única, não somente pelo uso da tecnologia e aparelhos maravilhosos que há no Centro de Reabilitação, mas também pelo carinho e acolhimento que todos os colaboradores oferecem aos pacientes. Isso faz toda a diferença”, afirma a especialista, que tem sua fala validada por José.

“Deus colocou pessoas escolhidas por Ele no meu caminho, no tempo certo e durante todo meu tratamento. Eu costumo dizer que este é o melhor hospital de América Latina. Já fui em vários lugares do Brasil, mas não existe outro igual. Aqui, as pessoas respeitam o paciente e nos tratam com muita dignidade. Somos todos seres humanos e se eu preciso ser bem tratado, eu devo tratar todos bem, e no Hospital de Amor eu recebo o melhor”, conta o paciente que revela não ter medo das agulhas que recebe uma vez por mês, durantes os 25 minutos de sessão.
Com quase dois anos de tratamento terapêutico de acupuntura, José não precisa mais do auxílio do andador e da bengala para caminhar. Aliado à acupuntura e atividades físicas prescritas pelo time do Centro de Reabilitação, ele decidiu se mudar para Barretos, onde pode receber um tratamento de qualidade, gratuitamente, o que não ocorre em seu estado de origem. Ao lado de sua fiel companheira, sua esposa Eliani, ele vive com seus oito filhos.
Picadas de Amor
“Costumo dizer que ganhar um beijo é melhor do que ganhar uma picada, porém, eu já tive crianças de 5 anos que pediram acupuntura e já tive idosos que tem um maior estresse, então é uma coisa muito pessoal. Tem pessoas que trazem medos, porque nós ocidentais, muitas vezes, achamos que a agulha significa punição e sofrimento, mas neste caso não, são agulhas do bem que trazem bem-estar”, conclui a Dra. Margareth.
Assim como no relato acima, existem diversas comprovações de que a acupuntura de fato funciona. Contudo, no Brasil essa terapia só dever ser utilizada de maneira complementar ao tratamento clínico orientado pelo médico, contribuindo para a qualidade de vida do paciente. É claro que também não pode faltar carinho, amor e empatia!

Você sabia que, no Brasil, o câncer de estômago é o quarto tipo mais frequente entre os homens e o sexto entre as mulheres? E que sua estimativa de novos casos, de acordo com o levantamento realizado pelo Instituto Nacional de Câncer (INCA), é de 21.290, sendo 13.540 em homens e 7.750 em mulheres? Mas afinal, qual a função do estômago e sua importância para o corpo humano?
O estômago é um órgão em forma de “J”, situado na parte superior do abdômen. Faz parte do sistema digestivo, cuja responsabilidade é processar os alimentos ingeridos, extraindo deles nutrientes (vitaminas, minerais, carboidratos, gorduras, proteínas e água). Os alimentos são conduzidos da garganta para o estômago, através de um tubo oco e muscular, chamado esôfago. Após deixar o estômago, os alimentos parcialmente digeridos passam para o intestino delgado e depois para o intestino grosso (cólon).
A parede do estômago é constituída por três camadas de tecido: a camada mucosa (que fica em contato com os alimentos), a camada muscular (camada média), e a camada serosa (externa, a que reveste o estômago).
E o que é o câncer do estômago?
O câncer de estômago (ou câncer gástrico) é o crescimento de células anormais no órgão desse sistema digestivo e pode ocorrer em qualquer local de sua extensão. Grande parte desse tipo de tumor ocorre na camada mucosa, surgindo na forma de pequenas lesões irregulares, com ulcerações (rompimento do tecido) – características de cânceres ou tumores malignos. Conforme a evolução da doença, essas células cancerígenas vão gradualmente substituindo o tecido normal do órgão, migrando para outras partes, podendo até chegar a outros lugares do organismo.
Com o pico de incidência em pessoas do sexo masculino de idade mais avançada (cerca de 65% dos pacientes diagnosticados com idade superior a 50 anos), o câncer de estômago se apresenta como o terceiro mais frequente entre homens e o quinto entre as mulheres. Dados do INCA revelam que o número de mortes por esse tipo de tumor chega a 14.314, sendo 9.207 em homens e 5.107 em mulheres.
Tipos de câncer de estômago
Os tumores de estômago se apresentam em três diferentes tipos: o adenocarcinoma – responsável por 95% dos tumores; o linfoma – diagnosticado em 3% dos casos; e o leiomiossarcoma – com início em tecidos que dão origem aos músculos e aos ossos.
Adenocarcinoma – é um tipo de câncer que possui características secretórias, se originando em tecidos glandulares.
Linfoma – é um tipo de câncer que tem origem nos linfonodos (gânglios) por todo o corpo, principalmente no timo, baço, amídalas, medula óssea e tecidos linfáticos no intestino. Assim como outros tipos de linfomas, eles são divididos em subtipos entre Linfoma de Hodgkin e Linfoma Não Hodgkin.
O linfoma do estômago apresenta uma incidência baixa (3%), podendo ser dividido em dois tipos:
– Linfoma Gástrico MALT: um tipo de linfoma associado à mucosa constituída por células pequenas e com baixo grau de malignidade.
– Linfoma de células grandes: com alto grau de malignidade, porém, com uma incidência muito rara (quando comparado ao primeiro).
Leiomiossarcoma – é um dos tumores benignos da musculatura lisa do estômago, geralmente também localizado em qualquer outro órgão. Sua incidência é baixa.
• Pólipos Gástricos
É o nome dado a um crescimento anormal de um tecido proveniente de uma membrana mucosa. Desenvolve-se nas cavidades de uma mucosa, podendo ter diferentes constituições e formatos. No estômago, os pólipos podem ser divididos em Adenoma e Pólipos Hiperplásicos.
– Adenoma: consiste em nódulos de epitélio displásico. Ocorrem quase que exclusivamente no antro (porção inicial do estômago), fazendo parte da Síndrome de Gardner (um transtorno genético que ocasiona a presença de múltiplos pólipos) ou gastrite crônica atrófica (condição em que as células da mucosa do estômago são diminuídas, prejudicando a produção do ácido gástrico responsável pela digestão dos alimentos).
A maioria dos carcinomas associados ao adenoma gástrico são maiores que 2 cm de diâmetro. Acredita-se que são necessários 10 a 15 anos para um adenoma se transformar em carcinoma.
– Pólipos Hiperplásicos: são os mais comuns pólipos do estômago (50 a 90% dos pólipos gástricos) e dois terços deles ocorrem no antro (porção inicial do estômago). A anormalidade básica é a hiperplasia (aumento excessivo do número de células) e eles se desenvolvem na mucosa gástrica atrófica. Pode haver associação com o Helicobacter pylori (também conhecido como ‘H. Pylori’). O tratamento é a remoção endoscópica ou cirúrgica.
• Tumores carcinoides
Representam 3% de todos os tumores carcinoides gastrointestinais. Existem três subtipos desse tumor no estômago:
– Carcinoide associado com gastrite atrófica crônica do tipo A com ou sem anemia perniciosa.
A gastrite do tipo A é causada por anticorpos contra as células parietais e o fator intrínseco, agindo na mucosa fúndica, causa atrofia glandular acloridria e eventualmente anemia perniciosa.
– Carcinoide associado com a síndrome de Zollinger-Ellison.
A síndrome de Zollinger-Ellison é o nome dado ao distúrbio causado por níveis excessivos do hormônio gastrina. A presença excessiva deste hormônio, por sua vez, faz o estômago produzir ácido clorídrico em excesso.
Esse distúrbio pode gerar um tipo de tumor que representa 8,6% dos tumores carcinoides gástricos e ocorrem quase que exclusivamente em pacientes com síndrome MEN-1 (Neoplasia Endócrina Múltipla). A hipergastrinemia está associada ao gastrinoma no pâncreas. O tratamento consiste em remover o gastrinoma ou a gastrectomia total.
– Tumor carcinoide de forma esporádica.
Não associados ao excesso de gastrina, esse tipo corresponde a 25% dos tumores carcinoides gástricos e têm um prognóstico pior que os tumores carcinoides associados à gastrite atrófica crônica e a síndrome de Zollinger-Ellinson. Como os tumores geralmente são grandes e a doença mais avançada, o tratamento necessita de cirurgia associada a radio e quimioterapia.
Sintomas do câncer de estômago
Estes sintomas podem caracterizar o câncer gástrico, mas outras condições ou doenças também podem causar os mesmos sintomas.
– Dor epigástrica (região central do abdômen – “boca do estômago”);
– Sensação de “estômago cheio” após as refeições e perda do apetite durante as refeições;
– Emagrecimento;
– Vômitos;
– Vômitos com sangue;
– Azia intensa;
– Diarreia;
– Constipação;
– Fadiga e Fraqueza;
– Fezes com sangue ou muito escurecidas (tipo borra de café);
– Dificuldade para se alimentar.
Deve-se tomar cuidado, pois esses sintomas muitas vezes não são percebidos pelos pacientes e só se tornam evidentes quando o tumor atinge um tamanho suficiente para diminuir o espaço de passagem do alimento.
Existem sintomas comuns em estágios avançados, como o emagrecimento intenso (caquexia) e pele e olhos amarelados pelo acúmulo do material metabólico de bilirrubina (icterícia). O paciente com câncer de estômago em estágios avançados também pode sentir dor quando o estômago é palpado.
Se você notar a persistência de qualquer desses sintomas, é necessário procurar um médico especialista na área gástrica, como um gastroenterologista.
Prevenção de câncer de estômago
Por ser um órgão que recebe diretamente os alimentos, a dieta é um fator essencial para a prevenção do câncer de estômago. O consumo excessivo de certos tipos de alimentos, suas conservações e a ausência de alguns deles, podem colaborar com a formação de um tumor.
Abaixo, relacionamos quais são essas condutas alimentares:
– Evitar a ingestão excessiva de nitritos e nitratos: os nitritos e nitratos podem ser encontrados em carnes e peixes em que se utiliza o método secagem para sua preservação – utilizado, por exemplo, em alimentos defumados. O nitrito, ao ser recebido no estômago, transforma-se em nitrosaminas, substâncias altamente cancerígenas.
– Evitar o consumo excessivo de alimentos enlatados, defumados, corantes ou alimentos conservados em sal.
– Evitar o consumo de alimentos guardados fora da geladeira ou mal conservados.
– Evitar o consumo de água com poços com altas concentrações de nitrato.
– Evitar uma alimentação carente das vitaminas A e C.
– Consumir carnes e peixes regularmente.
– Consumir frutas e verduras frescas, contendo ácido ascórbico e beta caroteno.
Esses elementos são benéficos por evitar que os nitritos se transformem em nitrosaminas.
Fatores de risco de câncer de estômago
Os fatores de risco para câncer gástrico incluem:
– Infecção do estômago por Helicobacter pylori (H. pylori), que são bactérias que vivem no estômago humano, responsáveis por alguns tipos de gastrite, úlcera e cancros. Seu formato permite atravessar com facilidade a camada de muco protetora do epitélio gástrico.
– Gastrite crônica (inflamação do estômago).
– Realização de cirurgia para úlcera.
– Anemia perniciosa: distúrbio que pode ocasionar facilitação ou dificuldade de absorção da vitamina B12 pelas células gástricas parietais (responsáveis pela liberação de ácido hidroclorídrico).
– Metaplasia intestinal: uma condição na qual o revestimento normal do estômago passa a ser do tipo de células que revestem o intestino.
– Polipose adenomatosa familiar (PAF): condição hereditária que gera inúmeros pólipos no intestino grosso.
– Pólipos gástricos.
– Tabagismo.
– Tabagismo associado ao consumo de álcool.
– Ter uma mãe, pai, irmã ou irmão que teve câncer de estômago.

Diagnóstico de câncer de estômago
O diagnóstico para esse tipo de câncer pode ser feito através de alguns exames:
– Exames de sangue (bioquímica): um procedimento em que uma amostra de sangue é coletada para medir a quantidade de certas substâncias liberadas no sangue, órgãos e tecidos do organismo. Uma quantidade alterada (superior ou inferior à normal) de uma substância pode ser um sinal de doença no órgão ou tecido que a produz. Nesse procedimento, o hemograma completo (um procedimento em que uma amostra do sangue é extraída e analisada) procura verificar:
– O número de glóbulos vermelhos (hemácias, que carregam o oxigênio), os glóbulos brancos (células de defesa) e plaquetas (responsáveis por ajudar a conter sangramentos).
– A quantidade de hemoglobina (proteína que transporta oxigênio) nas células vermelhas do sangue.
– Endoscopia: um procedimento para examinar o interior do esôfago, estômago e duodeno (primeira parte do intestino delgado), para verificar a ocorrência de áreas anormais. Um endoscópio (um tubo fino e iluminado) é passado através da boca e da garganta para o esôfago.
– Sangue oculto nas fezes: um teste para verificar a presença de sangue oculto nas fezes, que só pode ser visto com a ajuda de um microscópio. Pequenas amostras de fezes são colocadas em placas especiais e é feita a sua análise no laboratório.
– EED: é uma série de raios-x do esôfago e do estômago. O paciente bebe um líquido (contraste) que contém uma substância (bário) que os raios-X não conseguem atravessar, fazendo, desse modo, que seja possível enxergar melhor os órgãos a serem analisados. Este procedimento também pode ser chamado de seriografia gastrointestinal superior (seriografia do esôfago, estômago e duodeno) quando estes três órgãos são analisados.
– Biópsia: é a remoção de amostras de células ou tecidos para possibilitar a análise através de um microscópio, por um médico patologista, para verificar se há sinais de câncer ou algum outro tipo de doença. A biópsia geralmente é feita durante a endoscopia. Às vezes, uma biópsia pode mostrar alterações no estômago que não são câncer, mas que podem levar ao câncer.
– TC (Tomografia Computadorizada): é o exame no qual é feita uma série de imagens detalhadas de áreas no interior do corpo, tomadas de ângulos diferentes. As imagens são feitas por um computador ligado a uma máquina de raios-X. Um contraste pode ser injetado em uma veia, ingerido, ou ainda injetado através do reto para ajudar os órgãos ou tecidos a aparecem mais claramente.
Estadiamento do câncer de estômago
Alguns exames e procedimentos podem ser utilizados no processo de estadiamento da doença, entretanto, nem todos são necessários a todos os pacientes.
– Exames de β-hCG (Beta-gonadotrofina coriônica humana), CA-125 e CEA (Antígeno carcinoembrionário): são exames que medem os níveis de β-hCG, CA-125 e CEA no sangue. Essas substâncias são liberadas na corrente sanguínea, tanto por células sadias, quanto por células cancerígenas. Quando encontradas em quantidades mais elevadas do que normal, esses elementos podem representar um sinal de câncer gástrico ou outras doenças.
– Radiografia de tórax: é um raio X dos órgãos e ossos dentro do peito. Um raio-x é um tipo de raio de energia que pode atravessar o corpo e realizar um retrato de áreas dentro do corpo.
– Ultrassonografia endoscópica: é um procedimento em que um endoscópio é inserido no corpo, geralmente através da boca. Um endoscópio é um instrumento fino, de forma tubular, com uma luz e uma lente para a visão. A sonda na ponta do endoscópio é usada para produzir ondas sonoras de alta energia (ultrassom) e fazer ecos. Os ecos formam imagens dos tecidos do corpo possibilitando a avaliação do médico. Este procedimento também é chamado de endossonografia.
– TC (Tomografia Computadorizada): é o exame no qual são feitas uma série de imagens detalhadas de áreas no interior do corpo, tomadas de ângulos diferentes. As imagens são feitas por um computador ligado a uma máquina de raios-X. Um contraste pode ser injetado em uma veia, ingerido, ou ainda injetado através do reto para ajudar os órgãos ou tecidos a aparecem mais claramente.
– Laparoscopia: é um procedimento cirúrgico para olhar os órgãos dentro do abdômen para checar sinais de doença. Pequenas incisões (cortes) são feitas na parede do abdômen e um laparoscópio (um tubo fino e iluminado) é inserido em uma das incisões. Outros instrumentos podem ser inseridos através das incisões para realizar procedimentos, como a remoção de amostras de tecidos para pesquisas. Pode também, em alguns casos, realizar-se parte da cirurgia para tratamento por esse método.
– PET Scan (Tomografia por emissão de pósitrons scan): é um exame que combina a tomografia computadorizada e uma espécie de cintilografia. É utilizada uma substância radioativa (fluordesoxiglicose – FDG), que é injetada por uma veia e é mais absorvida por células tumorais, fazendo com que o câncer possa ser diagnosticado ou analisado com grande precisão.
Tratamento do câncer de estômago
Três tipos de tratamento são utilizados para o câncer de estomago. São eles:
– Cirurgia: é o tratamento mais comum para todos os estágios do câncer de estômago. Os seguintes tipos de cirurgia podem ser utilizados:
• Gastrectomia subtotal: remoção de parte do estômago que contém o câncer, linfonodos próximos, tecidos ou órgãos que possam estar acometidos pelo tumor.
• Gastrectomia total: remoção de todo o estômago, os linfonodos próximos, parte do esôfago, duodeno e outros tecidos próximos ao tumor. O baço pode ser removido. O esôfago é ligado ao intestino delgado para que o paciente possa continuar a comer e engolir. Se o tumor está obstruindo o estômago, mas o câncer não pode ser completamente removido por cirurgia, pode se realizar a colocação de uma prótese (um tubo fino e expansível), realizado através de endoscopia, a fim de manter uma passagem para o alimento.
– Radioterapia: a radioterapia é um tratamento contra o câncer que utiliza tipos de radiação para matar células cancerígenas ou impedi-las de crescer. Existem dois tipos de radioterapia: a terapia de radiação externa – a mais comum, que utiliza uma máquina para enviar radiação para o câncer; e a terapia de radiação interna (braquiterapia) – na qual a substância radioativa é colocada diretamente em contato com o tecido tumoral.
– Quimioterapia: um tratamento de câncer que usa medicamentos (remédios) para parar o crescimento das células cancerosas, matá-las ou impedi-las de se dividir. Quando a quimioterapia é tomada via oral ou injetada numa veia ou músculo, os remédios entram na corrente sanguínea e podem atingir as células cancerosas por todo o corpo (quimioterapia sistêmica). Quando a quimioterapia é colocada diretamente na coluna vertebral, um órgão ou uma cavidade do corpo, como o abdômen, as drogas afetam principalmente as células do câncer nessas áreas (quimioterapia regional). A forma como a quimioterapia é dada depende do tipo e estágio do câncer a ser tratado.


A quimioterapia é um dos principais tipos de tratamento no combate ao câncer. Trata-se de uma terapia que utiliza medicamentos para destruir as células doentes que formam um tumor. Estes remédios se misturam com o sangue e são levados a todas as partes do corpo, destruindo as células ruins que estão formando a doença e impedindo, também, que elas se espalhem pelo organismo.
Para esclarecer as principais dúvidas sobre a quimioterapia e sua importância na luta contra o câncer, eliminar os mitos envolvendo esse tipo de tratamento e ainda saber mais informações sobre seus efeitos colaterais, o Hospital de Amor traz uma entrevista exclusiva com o oncologista clínico da instituição, Dr. Luís Eduardo Zucca. Confira!
1) Qual é o principal objetivo da quimioterapia no tratamento de câncer?
R.: Existem 4 tipos de tratamento com quimioterapia:
• A quimioterapia neoadjuvante: esse tipo de quimioterapia é utilizado antes de um tratamento curativo para um tumor localizado. Geralmente, faz-se sessões de quimioterapia para tentar a redução do tumor e, assim, no tratamento curativo (seja ele com radioterapia ou cirurgia), o resultado ser mais efetivo e eficaz. Dessa forma, há menos riscos do desenvolvimento de comorbidades (surgimento de outras doenças em simultâneo) para o paciente.
• A quimioterapia adjuvante: utilizada após um tratamento curativo (seja ele em cirurgia ou radioterapia), tem o objetivo de diminuir e tentar matar todas as micrometástases (células cancerígenas se multiplicam num local distante para formar pequenos tumores) que possivelmente possam ter ficado no corpo, diminuindo assim as chances do câncer voltar.
• A quimioterapia paliativa: como o próprio nome diz, serve para paliar (amenizar) os sintomas dos pacientes. Podem ser pacientes que estejam com dor (proporcionando a melhora a deles com o uso da quimioterapia) e, por última instância, para melhorar a sobrevida com medicamentos quimioterápicos paliativos nos casos de pacientes com tumores metastáticos (quando o câncer se espalha além do local de origem para outras partes do corpo).
• A quimioterapia concomitante à radioterapia: nestes casos, a quimioterapia serve como um veículo para aumentar a potência da radioterapia.
2) Ela é indicada para quais tipos de tumores?
R.: A quimioterapia (seja ela neoadjuvante, adjuvante, paliativa ou concomitante à radioterapia) é indicada para a maioria dos tumores malignos.
3) Como é realizado o procedimento?
R.: Existem, basicamente, 2 tipos principais de procedimentos quimioterápicos: a quimioterapia intravenosa (pela veia), na qual o paciente é puncionado por uma veia periférica ou mesmo por um port-a-cath (dispositivo colocado pelo cirurgião dentro de uma veia mais calibrosa – aquelas com maior dilatação – no corpo do paciente); e a quimioterapia injetável, que é feita em ambientes preparados para receber a quimioterapia com um enfermeiro especializado. Geralmente, os pacientes ficam de 30 minutos até 6 horas fazendo quimioterapia intravenosa. Além disso, existem também as quimioterapias administradas por via oral, nas quais o paciente leva para casa os comprimidos orais e ingere de acordo com o esquema quimioterápico que o médico fornece para ele.
4) Existe mais de um tipo de quimioterapia?
R.: Existem vários tipos de quimioterapias, desde as específicas para certo tipo de tumor, até a quimioterapia que nós tratamos para uma variedade de tumores.
5) Existem efeitos colaterais na utilização da quimioterapia? Quais?
R.: As quimioterapias têm alguns efeitos colaterais manejáveis. Dependendo do esquema de quimioterapia que o paciente recebe, podem ocasionar náuseas, vômitos, cansaço, fadiga e baixa energia. A questão central, também dependendo do esquema de quimioterapia, é que geralmente os tratamentos quimioterápicos não matam apenas as células ruins, atingindo células boas que se multiplicam rapidamente (como cabelo e unha). Então, alguns esquemas quimioterápicos podem ocasionar a queda de cabelo e algumas alterações, mas também as células de defesa do nosso corpo. Dessa forma, em alguns casos, elas podem deixar o nosso corpo mais vulnerável a infecções.
6) Quando esses efeitos aparecem, o que é preciso fazer?
R.: Quando qualquer um desses efeitos aparecer é necessário procurar o seu médico e procurar o hospital. Por exemplo, para os pacientes que estão fazendo quimioterapia e têm febre, a primeira recomendação indicada é a procura do Hospital para passar pela avaliação do médico, pois como a quimioterapia também mata as células boas, o corpo fica vulnerável à infecção. Uma vez que o paciente tenha infecção e células de defesa baixa, nós, médicos, precisamos iniciar antibióticos e terapias o mais rápido possível. Mas, existem outros efeitos colaterais também manejáveis, como náuseas, vômitos, fadigas, inclusive queda de cabelo.
7) Qual é o tempo mínimo e qual é o tempo máximo de duração da quimioterapia?
R.: Existem vários tempos de quimioterapia, desde as que duram 15 minutos, como a blaumicina; aquelas que podem durar o dia inteiro, como a cisplatina; ou até a quimioterapia que o paciente vai para casa com um dispositivo e a quimioterapia fica correndo durante 48 horas dentro do seu organismo.
8) O paciente que é submetido a esse tipo de tratamento pode seguir sua rotina de atividades/trabalho normalmente?
R.: Dependendo do tipo de quimioterapia e do esquema quimioterápico, sim, é possível viver normalmente, inclusive trabalhando, estudando, fazendo as atividades diárias. Isso porque, hoje em dia, a maioria dos efeitos colaterais é bastante controlável, porém, sempre é necessário respeitar o próprio corpo.
9) Em média, quais são os custos da quimioterapia?
R.: O custo da quimioterapia também é variável, desde quimioterapias mais baratas, até aquelas que custam de 20 a 30 mil reais por mês.

Desde 2015, o Hospital de Amor conta com um programa de rastreamento para a detecção precoce do câncer colorretal – aquele que acomete o trato digestivo (intestino grosso e reto). De lá para cá, já foram alcançadas 12.723 pessoas, sendo 48 pacientes diagnosticados com esse tipo de tumor.
Conheça mais sobre o câncer colorretal, seus sintomas e saiba como se prevenir.
O que é câncer colorretal?
Os cânceres colorretais são aqueles que acometem o trato digestivo (intestino grosso e reto). Esses tumores são considerados mais passíveis de prevenção, pois a evolução natural deles é bem conhecida pela medicina: eles começam com lesões precursoras, ou seja, lesões pré-malignas (também conhecidas como pólipos) que são detectáveis e que podem ser removidas. Com essas medidas, é possível interromper a progressão da doença. Geralmente, as chamadas ‘lesões precursoras’ não apresentam sintomas (como sangramentos ou dores abdominais), por isso, para identificá-las, é necessário submeter o indivíduo a um rastreamento para prevenir a evolução da doença.
O que são pólipos?
São tumores benignos, parecidos com verrugas, que se desenvolvem na parte interna do cólon e reto. Cerca de 60% dos pólipos do intestino são adenomas e podem apresentar potencial para se tornarem tumores malignos. É importante que o diagnóstico e o tratamento sejam feitos precocemente, principalmente após os 50 anos e em caso de história de câncer colorretal na família.

Quais são os sinais e sintomas do câncer colorretal?
Os principais sintomas da doença são: mudança do hábito intestinal, isto é, constipação ou diarreia sem associação com o alimento ingerido; anemia sem causa aparente, principalmente em pessoas com idade acima de 50 anos; fraqueza; desconforto abdominal (com gases ou cólicas); emagrecimento intenso e inexplicável; sangramento pelo reto; e sensação de evacuação incompleta.
Qualquer pessoa que apresentar um desses sintomas deve procurar o médico, principalmente se houver sangramento anal, para que os exames clínicos necessários sejam realizados. Entre os exames estão: realização do toque retal e do exame de colonoscopia (procedimento de vídeo utilizado para visualizar o interior do intestino grosso e a parte final do intestino delgado).
Quais os fatores de risco para o desenvolvimento da doença?
Uma alimentação rica em carnes vermelhas, carnes processadas (como salsichas e mortadelas) e gorduras, além da ausência de atividade física regularmente (como o sedentarismo), ingestão abusiva de álcool, tabagismo, sobrepeso e obesidade, são alguns fatores externos que podem contribuir para o desenvolvimento da doença.
Pessoas com idade superior a 50 anos, ou que já tenham tido pólipos ou doença inflamatória intestinal, ou que tenham histórico de ocorrência de câncer colorretal em familiares, devem ficar atentas aos sinais.
Como se prevenir deste tipo de câncer?
Prevenir significa evitar os fatores que estão relacionados com o desenvolvimento de câncer colorretal. Adotar uma alimentação rica em frutas, verduras e vegetais, evitar o consumo de carnes vermelhas e embutidos, praticar exercício físico, evitar a obesidade, evitar o consumo de bebidas alcoólicas e cigarros, são importantes atitudes de prevenção. Os alimentos ricos em fibras protegem o intestino, pois facilitam a evacuação, aceleram o trânsito intestinal e diminuem o tempo de contato das substâncias carcinogênicas (que levam à formação do câncer) com a parede do intestino.
Refletir sobre os hábitos e estilo de vida é sempre uma forma de se prevenir de qualquer tipo de câncer e conquistar uma vida mais saudável. Confira algumas dicas:
– Praticar exercícios físicos regulares;
– Não fumar;
– Não ingerir bebidas alcóolicas;
– Não ingerir alimentos defumados, enlatados ou embutidos;
– Não ingerir alimentos com corantes e/ou conservantes;
– Se diagnosticado, remover pólipos através do exame de colonoscopia;
– Ingerir alimentos ricos em vitaminas C e E.
Porém, apesar de todos esses cuidados, também é necessário participar dos programas de rastreamento, pois essas medidas não são 100% eficazes. Existem dois exames que podem ser utilizados para rastrear esse tipo de tumor, sendo eles: o teste de imunoquímica fecal (conhecido também como teste FIT ou exame de sangue oculto nas fezes) e a colonoscopia (que é um exame de vídeo para visualizar o interior do intestino grosso e a parte final do intestino delgado). Recomenda-se iniciar o rastreamento a partir dos 50 anos, mas, cabe ao médico indicar qual é a melhor opção de procedimento para cada paciente.
Como é o teste FIT?
Também conhecido como exame de sangue oculto nas fezes, o teste FIT é indicado para um público bem específico: homens e mulheres que tenham entre 50 e 65 anos, que não tenham feito nenhum exame de colonoscopia ou de retossigmoidoscopia nos últimos 5 anos, não tenham nenhum histórico de doença inflamatória intestinal e de pólipos colorretais.
São necessárias três amostras de fezes consecutivas. Alguns dias antes do exame, alguns tipos de alimentos devem ser evitados. Além disso, medicamentos como AAS e anti-inflamatórios não devem ser tomados 7 dias antes do exame, e frutas cítricas e carne vermelha não devem ser consumidas três dias antes do procedimento. Se o resultado para o sangue oculto for positivo, será necessário realizar o exame de colonoscopia.
Como é a colonoscopia?
É um exame realizado por um aparelho de fibra ótica, longo (180 cm) e flexível, que é introduzido através do ânus e permite a visualização completa do reto e do cólon. Essa visualização ocorre por uma câmera inserida na extremidade do colonoscópio, cuja imagem é enviada para um monitor, permitindo assim, a análise simultânea do interior do cólon. O equipamento também permite a inserção de outros instrumentos especiais para a remoção de possíveis pólipos ou biópsias. O exame é feito sob sedação e analgesia, permitindo que o médico examine detalhadamente o cólon. Os riscos do procedimento são pequenos e estão vinculados ao sangramento depois da retirada de pólipos, biópsias e perfuração intestinal.
Como é tratamento para o câncer colorretal?
O tratamento para os tumores iniciais, geralmente, é menos agressivo, com a retirada de pólipos e lesões através da colonoscopia ou das cirurgias com ressecções locais dos tumores.
Nos tumores maiores do cólon, há a necessidade de cirurgia (convencional, laparoscópica ou robótica).
Nos tumores do reto, pode ser necessário realizar procedimentos radioterápicos e quimioterápicos antes da cirurgia.
Em resumo, o tratamento para o câncer colorretal envolve radioterapia, quimioterapia e/ou cirurgia, dependendo do local, do tamanho e da extensão da doença no cólon ou em outros órgãos (no caso de metástases – aparecimento do tumor em outros órgãos, como fígado ou pulmão, por exemplo). Quanto mais precocemente a doença for diagnosticada, menor a agressividade e o tempo de tratamento, proporcionando melhor qualidade de vida ao paciente.



Os milhares de pacientes que realizam tratamento no Hospital de Amor Barretos agora contam com uma nova alternativa de medicação para os tratamentos de cânceres de pulmão e melanoma (tipo mais grave de câncer de pele) em estágios avançados. Graças à parceria firmada com a farmacêutica MSD, a instituição poderá oferecer aos pacientes do Sistema Único de Saúde (SUS) o tratamento com a terapia anti-PD-1, conhecida como pembrolizumabe (Keytruda). O Hospital de Amor é a primeira entidade de saúde pública no Brasil a oferecer a imunoterapia.
A assinatura do termo aconteceu na última segunda-feira, dia 3 de setembro, reunindo médicos, o presidente do Hospital, Henrique Prata, e o diretor-geral do Centro Oncológico “Antônio Ermírio de Moraes” – Beneficência Portuguesa, de São Paulo, e membro do comitê de direção do Centro Oncológico do Hospital Israelita Albert Einstein, Dr. Antônio Buzaid.
De acordo com Buzaid, o tratamento imunoterápico é uma nova alternativa para a quimioterapia, além de possuir efeitos colaterais menores. “Quando aplicamos o Anti-PD-1, estimulamos uma sobrevida no paciente. Por isso, é tão importante investir em pesquisas clínicas para aumentar a receita da instituição e melhorar o tratamento básico. Para nós, o Hospital de Amor é um motivo de muito orgulho”, afirmou.
Para a diretora médica de oncologia da MSD Brasil, Dra. Márcia Datz Abadi, “o pembrolizumabe representa um avanço importante no tratamento do câncer e é um orgulho poder oferecer essa inovação aos pacientes do SUS. Nos sentimos honrados pela parceria e pioneirismo do Hospital de Amor”.
Após essa conquista, o HA poderá facilitar o acesso ao medicamento, acelerar o tratamento e as chances de cura e sobrevida dos pacientes. A estimativa é de que em duas semanas essa alternativa já esteja sendo aplicada na instituição. Segundo Henrique Prata, a assinatura do convênio representa um marco histórico nos mais de 50 anos de trajetória do Hospital e também para a oncologia brasileira. “Todas as pessoas têm direito de ter um tratamento digno. Portanto, temos muito o que comemorar com essa conquista”, declarou.

Câncer de Pulmão
O câncer de pulmão é considerado o mais comum e letal entre todos os tumores malignos. A estimativa do Instituto Nacional do Câncer (INCA) para este ano é de que 30 mil novos casos sejam diagnosticados no Brasil, sendo o de células não pequenas o mais comum – correspondente a 85% de todos os casos. Estimativas globais apontam que apenas 1% dos pacientes com câncer de pulmão avançado estão vivos, cinco anos após o diagnóstico.
Em junho, o Brasil se tornou o primeiro país do mundo a aprovar, baseado em um estudo de fase 3, o uso combinado de pembrolizumabe e quimioterapia para tratamento de pacientes com câncer de pulmão de células não pequenas (CPNPC) em estágio avançado ou metastático. De acordo com o estudo KEYNOTE-189, publicado no New England Journal of Medicine, o uso de pembrolizumabe associado à quimioterapia (pemetrexede e cisplatina ou carboplatina), quando utilizado em primeira linha de tratamento, reduz em 51% o risco de morte.
Para o oncologista clínico do HA, Dr. Pedro de Marchi, poder oferecer esse medicamento gratuitamente aos pacientes é um motivo de grande alegria. “Sem dúvida, estamos falando de um marco na história do Brasil. Com essa nova alternativa, a sobrevida é de 8 meses a 3 anos”, ressaltou.
O oncologista explica ainda que o Hospital de Amor recebe cerca de 600 novos pacientes com câncer de pulmão, por ano. Desses, 450 irão precisar de tratamento sistêmico. Entre eles, 360 possuem doença metastática. Desses, 320 não têm mutações. “Isso quer dizer que, desses 320 pacientes, 17% apresenta PD-L1 maior que 50% e seriam candidatos a esse tipo de tratamento, o que resultaria em, aproximadamente, 54 pacientes novos por ano”, finalizou Dr. Pedro de Marchi.
Câncer Melanoma
O melanoma é caracterizado pelo crescimento descontrolado de células que compõem a pele. A incidência deste tipo de câncer tem aumentado nas últimas quatro décadas. Só o Brasil registra, anualmente, cerca de 5.500 novos casos da doença e, aproximadamente, 1.547 óbitos, segundo o INCA. Esse tipo de câncer é considerado o mais comum entre jovens adultos, mas também pode ser diagnosticado em crianças, adolescentes e idosos.
De acordo com o estudo Keynote-001, em 655 pacientes com melanoma metastático, 34% de todos eles e 41% dos que não haviam tido qualquer tratamento prévio, permanecem vivos após 5 anos do uso de pembrolizumabe, em uma doença em que a quimioterapia oferecia apenas poucos meses de sobrevida. Já o estudo KEYNOTE-006 mostrou que 42% dos pacientes tratados com pembrolizumabe estavam vivos após quatro anos de diagnóstico.
“É trágico saber que somente pacientes que possuem convênios ou acesso aos atendimentos privados, conseguem ter acesso a esse tipo de tratamento. Agora, pela primeira vez, os pacientes do SUS, atendidos no Hospital de Amor, poderão contar com uma medicação inovadora. É uma luz de esperança para que, em pouco tempo, mais pacientes possam conseguir esta e todas as outras medicações que ainda não estão disponíveis gratuitamente”, declarou o oncologista clínico do HA, Dr. Sérgio Serrano.
O medicamento
O medicamento (pembrolizumabe) já pode ser utilizado no Brasil para o tratamento em primeira linha de melanoma avançado para pacientes com câncer de pulmão avançado, do tipo CPCNP, com expressão elevada ou moderada do biomarcador PD-L1 no tumor (expressão ≥50% ou 1%<49%) e tratamento de câncer urotelial (o mais comum é o câncer de bexiga). Ele também foi aprovado este ano para tratamento de câncer gástrico (o mais comum é o de estômago), após falha de duas terapias prévias.
A imunoterapia anti-PD-1 da MSD está sendo avaliada para mais de 30 tipos de tumores em 790 estudos clínicos. No Brasil, o medicamento está sendo pesquisado em mais de 29 ensaios clínicos, com cerca de 232 instituições envolvidas e mais de 500 pacientes em tratamento.

Publicado em 06 de set de 2018 | Artigos, Destaques, Institucional, Ensino e Pesquisa, Diagnóstico e Tratamento